2. 东北师范大学环境学院, 长春 130117;
3. 清华大学环境学院水质与水生态研究中心, 北京 100084
2. School of Environment, Northeast Normal University, Changchun 130117;
3. School of Environment, Tsinghua University, Beijing 100084
砷是一种有毒并致癌的化学元素, 普遍存在于各种环境介质和生物体中, 不仅会对生态环境造成严重影响, 还能通过食物链进入人体内, 危害人体健康(Smedley et al., 2002).东南亚及南亚是亚洲地下水砷污染最严重的地区, 据估计区域内有超过1亿以上的人群在饮用砷含量高于世界卫生组织限值(10 μg·L-1)的饮用水(Flanagan et al., 2012).近年来, 国外许多研究表明该区域的高砷地下水与相应河流相互影响, 包括恒河、湄公河及红河等(Buschmann et al., 2009; Chakraborti et al., 2003).尽管区域中大多数河流发源于我国青藏高原, 但多数研究都集中在区域水体中砷的分布及影响, 对上游源头区域西藏水体中砷的研究较为有限.西藏狮泉河流域和雅鲁藏布江流域水体中砷的富集与当地高砷热泉及盐湖有关, 沉积物对As的吸附能力较强(Li et al., 2013).此外, 王明国等(2012)对两个流域内的水体进行采集分析, 发现43.2%的河水样品中砷含量高于10 μg·L-1.虽然西藏目前尚未有饮水型砷中毒的报道, 但地表水中砷含量异常无疑是对流域内居民饮水安全的潜在危害, 对居民的生命健康存在极大的威胁.因此, 研究沉积物对砷的吸附解吸特征, 探究砷在沉积物-水之间的迁移及其影响因素, 对于保障居民饮水安全具有重要意义.
澜沧江-湄公河是著名的国际河流, 自北而南流经6个国家, 总长4909 km; 中国境内澜沧江全长2139 km, 流经青海、西藏、云南三省.澜沧江干流从源头至昌都为上游段, 昌都至功果桥为中游段, 功果桥至南阿河口为下游段(何大明等, 2014).近年来, 澜沧江由于不合理的矿山开采以及梯级水电站的修建, 造成了重金属污染、泥沙淤积和水生生物减少等水环境及水生态问题, 已引起了下游国家乃至国际社会的关注(张娟等, 2000;张继来等, 2014; 傅开道等, 2016).
昂曲是澜沧江最大的支流, 在昌都与扎曲汇合成澜沧江.本文选取西藏昂曲昌都水电站库区表层沉积物作为研究对象, 通过模拟实验研究pH、温度、流速、共存离子、溶解氧、粒径和颗粒物浓度等水环境因子对砷吸附解吸性能的影响, 对预测砷在下游水体中的环境效应具有一定指导意义, 为揭示该区域砷在沉积物-水界面的迁移机制及预防饮水型砷中毒提供科学依据及理论基础.
2 材料与方法(Materials and methods) 2.1 实验材料 2.1.1 实验试剂及实验仪器主要实验试剂:十二水砷酸钠、亚砷酸钠、硫酸亚铁、硫酸锰、硫脲、抗坏血酸、硼氢化钠、盐酸、硝酸和氢氧化钠等均为分析纯, 购自国药集团化学试剂有限公司.
实验仪器:多参数分析仪(DZS-706, 雷磁)、原子荧光光谱仪(AF-610B, 北京北分瑞利分析仪器有限责任公司)、微波消解仪(MARS Xpress, CEM)、电感耦合等离子体质谱仪(ICP-MS, Agilent 7800a)、恒温摇床(HZY-E, 金坛经济开发区吉特实验仪器厂)、高速冷冻离心机(3-18KS, Sigma)、紫外分光光度计(U-3900, 日本日立)、激光粒度分析仪(Mastersizer analyzer 2000, 英国马尔文公司).
2.1.2 沉积物样品的采集与处理沉积物样品于2018年12月采集于西藏昂曲昌都水电站库尾2 km处, 根据随机布点混合的方法, 采集河床表层0~20 cm沉积物.沉积物冷冻干燥后, 剔除石砾、植物根系等明显异物, 依次过10目、35目、60目和230目的筛网, 得到4种不同粒级的沉积物样品:500~2000、250~500、63~500、< 63 μm, 装袋贴标签于室温下保存备用.
取(0.5±0.0005) g沉积物样品置于消解管中, 依次加入2 mL硝酸和6 mL盐酸, 待反应结束后将消解管放置于微波消解仪中, 经微波消解后用ICP-MS测定不同粒径沉积物的金属含量;采用水合热重铬酸钾氧化-比色法(鲁如坤, 2000)测定沉积物的有机质含量.以上实验重复2次, 并做空白试验, 沉积物金属含量平行样的相对误差 < 5%.使用激光粒度仪对沉积物粒径分布特征进行分析.
2.2 实验方法 2.2.1 吸附正交实验为了考察河流水环境因子, 例如河水流速、溶解氧、上游来水中As含量以及共存铁锰等金属离子含量、颗粒物浓度、季节温度变化等对As吸附过程的影响, 本试验以pH值、转速、溶解氧、Fe、Mn含量、颗粒物浓度、温度、粒径及As含量为实验因子, 评估不同条件下As的吸附量.
为确保实验中各因子的设定符合研究区域实际情况, 保证实验的科学性及合理性, 对昂曲河流和昌都水库的水体进行分析检测.昂曲水体中As(Ⅲ)与As(Ⅴ)的浓度比约为1 : 4, 为了使模拟实验As的浓度包含实际情况, As的浓度设置为50~4000 μg·L-1;pH范围在7~9之间, 因此设置pH=7、9两种条件;Fe、Mn浓度分别为40~300和2~30 μg·L-1, 且比例大致为10 : 1, 因此分别设置了Fe、Mn浓度及比例分别为200 : 20、600 : 30以及1200 : 30 3种模拟条件;水体颗粒物浓度为0.01~1.5 g·L-1, 因此分别设置0.2、1、1.5 g·L-1 3种模拟条件;由于水体可能出现的兼氧、好氧等状况, DO设置为兼氧条件(1 mg·L-1)和好氧条件(3 mg·L-1、6 mg·L-1);为模拟一年内水体不同温度变化的影响, 设置0.5 ℃(冬季)、5 ℃、10 ℃(春、秋季)以及20 ℃(夏季)4种温度模拟条件;同时综合考虑水流流速, 选用转速范围0~100 r·min-1, 根据锥形瓶半径和转速, 可知锥形瓶内溶液的线速度为0~0.88 m·s-1, 与水库水体的实际流速相近.吸附正交试验因素水平表见表 1.
| 表 1 吸附正交试验因素水平表 Table 1 Factor level table of adsorption orthogonal test |
如表 1所示, 本试验有1个因素2水平、4个因素3水平以及3个因素4水平, 没有直接对应的正交表可用.因此采用拟水平法, 将B因素的第二水平、C因素的第三水平、D因素的第三水平、E因素的第二水平进行重复, 采用L32(2×47)正交表进行正交试验.虽然拟水平后的表对所有因素来说不具有均衡搭配的性质, 但仍具有部分均衡搭配的性质, 因此拟水平法保留了正交表的优点(岳学军等, 2015).
用砷酸钠(Na3AsO4·12H2O)和亚砷酸钠(NaAsO2)配制400 mg·L-1的As溶液作为储备液, 其中As(Ⅲ)与As(Ⅴ)的浓度比为1 : 4;用硫酸亚铁(FeSO4)和硫酸锰(MnSO4)配制Fe、Mn储备液, Fe(Ⅱ)、Mn(Ⅱ)浓度分别为1200、30 mg·L-1.
根据吸附正交试验设计表中所列实验条件(表 4), 用上述储备液在250 mL具塞锥形瓶中配制100 mL水样, 并用0.1 mol·L-1的NaOH和HCl调节pH值, 通过曝入氮气(N2)或氧气(O2)调节溶液的溶解氧含量.准确称取沉积物置于250 mL具塞锥形瓶中, 将锥形瓶置于恒温摇床中振荡6 h后, 取一定体积溶液离心并用0.45 μm水系滤膜过滤.用氢化物发生-原子荧光光谱仪对As浓度进行测定, 吸附量由起始浓度及平衡浓度的差值计算, 吸附量的计算公式如式(1)所示.实验重复2次, 并做空白试验.
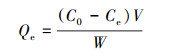
|
(1) |
| 表 4 吸附正交试验设计及结果 Table 4 Design and results of adsorption orthogonal test |
式中, Qe为吸附平衡时砷的吸附量(mg·kg-1);C0为砷溶液的初始浓度(mg·L-1);Ce为吸附平衡时溶液中砷的浓度(mg·L-1);W为沉积物质量(g);V为溶液体积(L).
2.2.2 等温吸附实验取一定体积As、Fe、Mn储备液于250 mL具塞锥形瓶中混合并稀释, 配制As浓度为5、10、20、50、80、100 μg·L-1的溶液, 溶液中Fe、Mn浓度分别为600、30 μg·L-1, 调节pH至8.7、DO浓度至3 mg·L-1.准确称取一定量 < 63 μm粒径沉积物加入锥形瓶中, 使溶液中颗粒物浓度分别为0.20、0.50、1.00 g·L-1.将锥形瓶置于恒温摇床中, 在10 ℃下以100 r·min-1振荡6 h, 离心过滤后用氢化物发生-原子荧光光谱仪测定As的浓度, 并计算其吸附量.实验重复2次, 并做空白试验.
2.2.3 解吸正交实验为考察沉积物在不同环境下的释放量, 以pH、转速、DO、温度、颗粒物浓度及粒径为实验因子, 评估As的解吸量, 实验因子根据现场实测数据取值.选用L12(25×4)型正交表进行实验设计, 共有5个因素2水平和1个因素4水平, 详见表 2.
| 表 2 解吸正交试验因素水平表 Table 2 Factor level table of desorption orthogonal test |
根据解吸正交试验设计所列出的实验条件(表 6), 向250 mL具塞锥形瓶中加入100 mL超纯水, 用NaOH和HCl调节pH, 通过曝入N2或O2调节溶液的溶解氧含量, 准确称取一定量沉积物加入其中.将锥形瓶置于恒温摇床中振荡24 h, 取一定体积溶液离心并用0.45 μm水系滤膜过滤.用氢化物发生-原子荧光光谱仪对As浓度进行测定, 实验重复2次, 并做空白试验.解吸量的计算公式如式(2)所示.
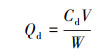
|
(2) |
| 表 6 解吸正交试验设计及结果 Table 6 Design and results of desorption orthogonal test |
式中, Qd为解吸平衡时砷的解吸量(mg·kg-1);Cd为解吸平衡时溶液中As的浓度(mg·L-1); W为沉积物的质量(g);V为溶液体积(L).
3 结果与讨论(Results and discussion) 3.1 沉积物样品的基本特征昂曲不同粒径沉积物中金属含量和有机质含量如表 3所示.不同粒径沉积物中砷含量由大到小依次为:(63~250 μm)>(< 63 μm)>(500~2000 μm)>(250~500 μm).不同粒径沉积物中砷含量为10.70~35.18 mg·kg-1, 原始沉积物中砷含量为27.04 mg·kg-1.根据杜光伟等(2001)研究, 西藏三江地区河流沉积物中砷的平均含量为19.5 mg·kg-1, 张银烽(2016)对三江流域的沉积物研究表明沉积物中砷的平均含量为17.3 mg·kg-1, 与本研究中沉积物的砷含量结果相近.
| 表 3 沉积物样品的特征 Table 3 Characteristics of sediment samples |
本研究采用极差分析法对正交试验结果进行分析, Ki为某一水平下As吸附量的平均值, 极差R的大小可以确定各个因素对试验指标的影响程度, 极差越大说明该因素对试验指标的影响越大, 分析结果见表 4.各因素对As吸附量的影响程度由高到低依次为:As含量>颗粒物浓度>粒径>温度>Fe、Mn含量>DO>转速>pH.
As初始含量和颗粒物浓度是对As吸附量影响最大的两个因素, 均与As吸附量有显著相关性.As吸附量随初始As含量的增大而增大, 这与Yavuz等(2003)的研究结果一致.当颗粒物浓度从0.20 g·L-1逐渐升高至1.50 g·L-1, Ki减少且幅度较大, 表明沉积物对As的吸附存在明显的固体浓度效应(Santschi et al., 1997; 王晓丽等, 2010).
研究表明, 沉积物的粒径越小, 对As的吸附能力越强(Lombi et al., 2000).在本试验中63~250 μm粒径沉积物, Ki=519.28 mg·kg-1, 远高于其它粒径沉积物的吸附量, 除了沉积物粒径的影响因素, 还与沉积物中有机质含量有关.沉积物中的有机质可以与一系列金属离子形成简单络合物及混合配位络合物, 使沉积物吸附能力增强(Bertin et al., 1995; Lombi et al., 2000; Twardowska et al., 2003; PhanitRatasuk et al., 2003).从表 3可知, 63~250 μm粒径沉积物中有机质含量最高(3.13 g·kg-1), 故该粒径沉积物对As的吸附能力较强.可见, 沉积物中有机质含量是影响其对As吸附性能的重要因素之一.
pH不但能影响砷的存在形态, 还能通过改变颗粒物的表面电荷来影响颗粒物对As的吸附能力, 是砷迁移转化的重要因素(胡立刚等, 2009; 曹明莉等, 2016).沉积物对As的平均吸附量Ki随着pH值的增大而增大(图 1), 表明在中性及弱碱性环境下, pH值的升高有利于As的吸附.这可能是由于在好氧条件下, pH升高促进了水中Fe(Ⅱ)、Mn(Ⅱ)形成(氢)氧化物, 吸附或结合As并沉淀, 导致吸附量增大(Deng et al., 2014).
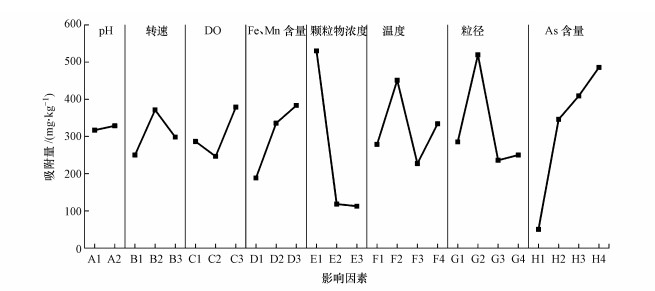 |
| 图 1 吸附正交试验各因素的影响 Fig. 1 Influence of various factors in adsorption orthogonal test |
随着吸附体系内Fe、Mn含量的上升, Ki从118.32 mg·kg-1增大至383.44 mg·kg-1.这是因为铁、锰的氧化物和氢氧化物能通过表面配位反应吸附水体中的砷, 从而增加沉积物吸附砷的能力(李雪等, 2011).显然, 水中Fe、Mn含量增大能显著增大沉积物对As的吸附量.
DO、温度及转速对As的吸附量无显著影响.由图 1可知, 随着DO逐渐增大, 吸附量先降低后升高, 无明显规律, 但仍能观察到DO为6 mg·L-1时As吸附量最高, 表明好氧条件有利于沉积物对As的吸附, 这可能与铁锰被氧化吸附或结合As有关.随着转速与温度逐渐增大, Ki值均呈现先上升后下降的趋势, 前者可能是由于沉积物与As的结合并不牢固, 过大的转速影响液体剪切力, 导致吸附能力降低;后者可能是离子交换能力增强与分子吸附能力降低相互作用所导致, 该现象与佘海燕(2005)的研究结果一致.
综上, 沉积物对砷的吸附量随着吸附体系内As含量、pH和Fe、Mn含量的增大而增大, 随颗粒物浓度的增大而减少, DO、温度及转速对As吸附量的影响不显著;沉积物中有机质含量是影响不同粒径沉积物对As吸附性能的重要因素之一.
3.3 吸附等温线当吸附达到平衡时, 沉积物对重金属的吸附量与溶液中重金属离子的平衡浓度之间的关系可以用吸附等温曲线来描述, 常用的拟合模型为Langmuir和Freundlich吸附等温式, 其表达式见式(3)、(4).
Langmuir吸附等温式:
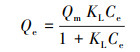
|
(3) |
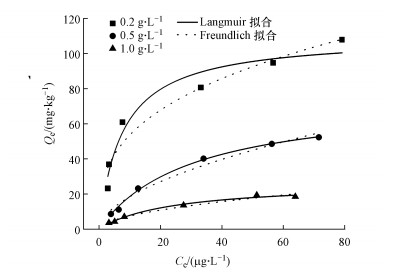
Freundlich吸附等温式:
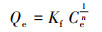
|
(4) |
式中, Ce为吸附平衡时溶液中砷的质量浓度(μg·L-1); Qe为吸附平衡时沉积物对砷的吸附量(mg·kg-1); Qm为单位表面上达平衡时的最大吸附量(mg·kg-1); KL为与吸附能吸附热有关的常数, 其值越大表示吸附能力越强; Kf、n为经验常数.
图 2为As在不同颗粒物浓度条件下的吸附等温线, 分别用Langmuir和Freundlich模型对图 2中吸附等温线进行拟合, 拟合结果见表 5.由表 5可知, Langmuir和Freundlich模型均能较好地拟合As在沉积物上的吸附过程, 表明该温度下沉积物对As的吸附既有物理吸附也有化学吸附.Freundlich型吸附等温式拟合1/n值均小于1, 说明吸附过程表现出一定的非线性(王新等, 2013).Langmuir模型对不同颗粒物浓度的吸附等温线拟合效果较好(R2=0.957~0.997), 而采用Freundlich模型拟合效果相对较差(R2=0.947~0.976), 说明沉积物对As的吸附属于单分子层吸附.拟合得出最大吸附量Qm值为26.53~110.13 mg·kg-1, 随颗粒物浓度的增大而下降, 存在明显的固体浓度效应, 与吸附正交试验的研究结果一致.许多报道中均发现了固体浓度效应, 目前对其产生原因尚未达成共识, 尽管经典吸附等温式能有效描述不同颗粒物浓度下的吸附实验结果(R2>0.99), 但其模型参数值均与颗粒物浓度相关(Santschi et al., 1997; Chen et al., 2007; 赵凌曦, 2013; 郭亚利, 2014).在本研究中, 随着颗粒物浓度增大, Qe、Kf和1/n均降低, KL增大, Langmuir和Freundlich模型参数均对颗粒物浓度具备依赖性, 与其理论相悖, 表明不能用于描述或预测实际吸附体系所观察到的固体浓度效应(郭亚利, 2014).但从图中仍可观察到, 随颗粒物浓度的增大, 达到吸附平衡的速度越快(曲线趋于平缓), 这是因为颗粒物浓度增大提供了更多的吸附位点, 促使吸附更快达到平衡.
 |
| 图 2 砷在沉积物上的吸附等温线 Fig. 2 Adsorption isotherm of arsenic on sediments |
| 表 5 Langmuir和Freundlich模型拟合参数 Table 5 Langmuir and Freundlich model fitting parameters |
从表 5的极差分析结果可知, 各因素对As解吸量的影响程度由高到低依次为:粒径>颗粒物浓度>DO>转速>pH>温度.
粒径是影响解吸量的重要因素, 由图 3可知, 不同粒径的解吸量从大到小依次为:(< 63 μm) >(63~250 μm) >(500~2000 μm)>(250~500 μm).从表 3、图 3可知不同粒径的解吸量与沉积物的性质有关, 除了与其自身As含量有关, 还与有机质含量有关.As含量越高, 能被解吸的As就越多;沉积物中有机质含量越高, 解吸能力越弱.250~500 μm和500~2000 μm粒径沉积物的As含量相近, 但250~500 μm沉积物中有机质含量较高(1.68 g·kg-1), 解吸能力较弱, 因此250~500 μm粒径沉积物平均解吸量最小.可见, 不同粒径沉积物的解吸量是As含量与有机质含量综合作用的结果.
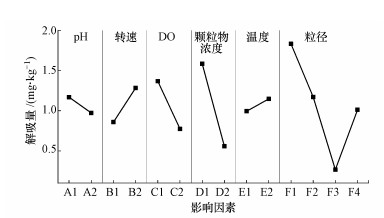 |
| 图 3 解吸正交试验各因素的影响 Fig. 3 Influence of various factors in desorption orthogonal test |
颗粒物浓度、DO以及pH均与As的解吸量呈负相关.随着颗粒物浓度的上升, 解吸量显著下降.当DO为0时As解吸量较高, 表明厌氧环境更利于As的解吸, 因为在厌氧环境下, 沉积物中铁锰氧化物还原溶解并释放砷;而在好氧环境下, 解吸到水中的Fe(Ⅱ)、Mn(Ⅱ)被氧化形成Fe(Ⅲ)、Mn(Ⅳ)(氢)氧化物, 吸附As或与As共沉淀, 从而降低了解吸能力(杨芬等, 2015).pH值升高亦能促进这一过程, 使水中铁锰更易形成氢氧化物从而吸附As, 因此As解吸量随pH的增大而减少.
由图 3可知, 温度和转速与As的解吸量呈正相关, 当温度与转速逐渐增大时, Ki亦随之增大.表明在一定范围内, 温度上升与转速提高均有利于As从沉积物中解吸到水中.据此可推测在夏季温度较高、水流流速较快的环境下, 沉积物中的As更易释放到水中.
综上, As解吸量随着解吸体系温度及转速的增大而增大, 随着DO、pH及颗粒物浓度的增大而减小;不同粒径沉积物的解吸量主要与沉积物自身As含量及有机质含量有关.
4 结论(Conclusions)1) 吸附正交实验的结果表明, 各因素对砷吸附量的影响程度由高到低依次为:As含量>颗粒物浓度>粒径>温度>Fe、Mn含量>DO>转速>pH.沉积物对砷的吸附量随着初始As含量、Fe、Mn含量和pH的增大而增大, 随着颗粒物浓度的增大而减小;不同粒径沉积物对砷的吸附能力与沉积物的有机质含量有关, 有机质含量越高, 吸附能力越强.
2) 吸附等温线用Langmuir和Freundlich模型拟合均能得到较好的拟合结果, 拟合得出最大吸附量Qm的值为26.53~110.13 mg·kg-1, 不同颗粒物浓度的吸附等温线表明沉积物对As的吸附存在固体浓度效应.
3) 解吸正交实验的结果表明, 各因素对砷解吸量的影响程度由高到低依次为:粒径>颗粒物浓度>DO>转速>pH>温度.不同粒径沉积物的解吸量与其自身砷含量及有机质含量有关, As解吸量与沉积物砷含量呈正相关关系, 与有机质含量呈负相关关系.As解吸量随转速和温度的增大而增大, 随着pH、DO和颗粒物浓度的增大而减小, 表明在夏季温度较高、径流量较大的环境下, 沉积物中的As更容易释放到河流水体中, 增大了水体生物和人类健康安全危险.
Bertin C, Bourg A C M. 1995. Trends in the heavy metal content (Cd, Pb, Zn) of river sediments in the drainage basin of smelting activities[J]. Water Research, 29(7): 1729-1736. DOI:10.1016/0043-1354(94)00327-4 |
Buschmann J, Berg M. 2009. Impact of sulfate reduction on the scale of arsenic contamination in groundwater of the Mekong, Bengal and Red River deltas[J]. Applied Geochemistry, 24(7): 0-1286. |
Chakraborti D, Mukherjee S C, Pati S, et al. 2003. Arsenic groundwater contamination in Middle Ganga Plain, Bihar, India:A Future Danger?[J]. Environmental Health Perspectives, 111(9): 1194-1201. DOI:10.1289/ehp.5966 |
Chen X, Wu W, Shi J, et al. 2007. Adsorption of copper and zinc on Pseudomonas putida CZ1:particle concentration effect and adsorption reversibility[J]. Colloids Surf B Biointerfaces, 54(1): 46-52. DOI:10.1016/j.colsurfb.2006.07.009 |
曹明莉, 盛智博, 张会霞. 2016. 溶液pH值对石墨烯及其复合材料吸附重金属离子的影响[J]. 功能材料, 47(9): 9051-9056. |
杜光伟, 徐开锋. 2004. 藏东"三江"地区地球化学特征及其找矿意义[J]. 物探与化探, 25(6): 425-431. |
Deng T, Wu Y, Yu X, et al. 2014. Seasonal variations of arsenic at the sediment-water interface of Poyang Lake, China[J]. Applied Geochemistry, 47: 170-176. DOI:10.1016/j.apgeochem.2014.06.002 |
Flanagan, Sara V, Johnston, et al. 2012. Arsenic in tube well water in Bangladesh:health and economic impacts and implications for arsenic mitigation[J]. World Health Organization. Bulletin of the World Health Organization, 90(11): 839-846. DOI:10.2471/BLT.11.101253 |
傅开道, 王超, 苏斌, 等. 2016. 澜沧江中下游水库泥沙重金属分布及其污染评价[J]. 生态经济, 32(12): 163-168, 191. |
郭亚利.2014.固体浓度对固-液界面吸附的影响[D].济南: 山东大学
|
何大明. 1995. 澜沧江——湄公河水文特征分析[J]. 云南地理环境研究, 7(1): 58-74. |
胡立刚, 蔡勇. 2009. 砷的生物地球化学[J]. 化学进展, 21(Z1): 458-466. |
Lombi E, Sletten R S, Wenzel W W. 2000. Sequentially extracted arsenic from different size fractions of contaminated soils[J]. Water Air and Soil Pollution, 124(3/4): 319-332. DOI:10.1023/A:1005230628958 |
鲁如坤. 2002. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社.
|
李雪, 王颖, 张笛. 2011. 河口沉积物对砷的吸附性能及影响因素[J]. 环境科学与技术, 34(12): 1-6. |
Li S, Wang M, Yang Q, et al. 2013. Enrichment of arsenic in surface water, stream sediments and soils in Tibet[J]. Journal of Geochemical Exploration, 135: 104-116. DOI:10.1016/j.gexplo.2012.08.020 |
Ratasuk P, Parkpian P, Jugsujinda A, et al. 2003. Factors governing adsorption and distribution of copper in samut prakarn coastal sediment, Thailand[J]. Environmental Letters, 38(9): 1793-1810. |
Santschi P H, Lenhart J J, Honeyman B D. 1997. Heterogeneous processes affecting trace contaminant distribution in estuaries:The role of natural organic matter[J]. Marine Chemistry, 58(1): 99-125. |
Smedley P L, Nicolli H B, Macdonald D M J, et al. 2002. Hydrogeochemistry of arsenic and other inorganic constituents in groundwaters from La Pampa, Argentina[J]. Applied Geochemistry, 17(3): 259-284. |
佘海燕. 2005. 河湖沉积物对重金属吸附-解吸的研究概况[J]. 化学工程师, (7): 33-36. |
Twardowska I, Kyziol J. 2003. Sorption of metals onto natural organic matter as a function of complexation and adsorbent-adsorbate contact mode[J]. Environment International, 28(8): 0-791. |
王晓丽, 郭博书. 2010. 黄河沉积物对磷酸盐吸附的固体浓度效应研究[J]. 内蒙古师范大学学报(自然科学汉文版), 39(1): 60-63. |
王明国, 李社红, 王慧, 等. 2012. 西藏地表水中砷的分布[J]. 环境科学, 33(10): 3411-3416. |
王新, 杨晓芳, 王东升, 等. 2013. 铊在河流沉积物上的吸附解吸行为研究[J]. 环境科学学报, 33(2): 535-543. |
Yavuz O, Altunkaynak Y, Güzel F. 2003. Removal of copper, nickel, cobalt and manganese from aqueous solution by kaolinite[J]. Water Research, 37(4): 948-952. DOI:10.1016/S0043-1354(02)00409-8 |
岳学军, 全东平, 洪添胜, 等. 2015. 柑橘叶片叶绿素含量高光谱无损检测模型[J]. 农业工程学报, 31(1): 294-302. |
杨芬, 朱晓东, 韦朝阳. 2016. 陆地水环境中砷的迁移转化[J]. 生态学杂志, 34(5): 1448-1455. |
赵凌曦.2013.固-液界面吸附中的吸附剂浓度效应研究[D].济南: 山东大学
|
张娟, 许金泉. 2000. 兰坪沘江中砷污染的化学形态及迁移转化规律[J]. 昆明理工大学学报(自然科学版), 25(2): 75-80. |
张继来, 傅开道, 王波, 等. 2014. 澜沧江河床沉积物重金属污染评价[J]. 地理科学进展, 33(8): 1136-1144. |
张银烽.2016.源于青藏高原流域中砷的富集、迁移转化规律及其环境效应研究[D].北京: 中国科学院大学
|
 2020, Vol. 40
2020, Vol. 40


