近年来, 随着制药行业的迅速发展, 制药废水的排放问题也日渐突出.由于生产工艺复杂、原料种类繁多, 制药废水通常具有有机物浓度高、成分复杂、毒性大、可生化性差等特点, 属于难降解的工业废水之一(Gadipelly et al., 2014).2015年国务院发布的《水污染防治行动计划》将制药行业归入专项整治的十大重点行业, 国家和地方制定的制药废水排放标准也日益严格, 制药企业废水治理的难度随之增大.然而, 由于制药废水的可生化性差, 经一级预处理和二级生物处理后, 其二级出水中往往具有较高浓度的难降解有机物, 直接排放会增加水体的生态风险并影响水生生物的生长(Shi et al., 2017).因此, 对制药废水二级出水进行深度处理是非常必要的.
常见的深度处理技术主要包括活性炭吸附(Cimbritz et al., 2019)、膜分离(Chew et al., 2018)、生物处理技术(Li et al., 2019)及高级氧化技术等, 其中, 高级氧化技术(Advanced oxidation processes, AOPs)由于具有氧化效率高、占地小、无二次污染等优点而成为废水深度处理领域的研究热点之一.常见的AOPs工艺包括臭氧氧化(Hansen et al., 2016)、芬顿及类芬顿氧化(Jain et al., 2018;Guan et al., 2018)、光催化氧化(Mano et al., 2015;袁宏林等, 2019)、电化学氧化(Silva et al., 2017)及多种高级氧化的集成工艺(Xiao et al., 2015;Sengul et al., 2017;Fan et al., 2017).研究表明, 将光催化与芬顿氧化耦合的光芬顿工艺能够实现更高的降解效率(Bai et al., 2016;Rott et al., 2017).然而, 现有的光芬顿相关研究大多聚焦于对模拟污染物的降解机制和催化行为, 缺乏对实际废水的处理研究;此外, 关于光芬顿反应器的设计和研究较少, 缺少大规模的可实际应用的反应器, 限制了光芬顿技术在工业废水深度处理领域的应用(Qanbarzadeh et al., 2021).
基于上述研究背景, 本文以实际制药企业的二级出水为研究对象, 通过小试试验对比UV/TiO2、UV/H2O2、UV/TiO2/H2O2 3种AOPs技术的处理效果, 在此基础上利用自主设计的一体化光催化装置进行连续动态试验, 研究光芬顿处理前后有机物含量、有机物特性、生物毒性等性质的变化, 以期为光芬顿深度处理工艺的实际应用提供理论及技术支撑.
2 材料和方法(Materials and methods) 2.1 试剂与材料本研究以浙江省宁波市某生物制药企业生化处理后的二沉池出水为研究对象, 该企业废水处理量约为160 m3·d-1.经0.7 μm玻璃纤维滤膜过滤后该二级出水的主要水质指标见表 1.
| 表 1 制药废水二级出水的水质特征 Table 1 Characteristics of the pharmaceutical secondary effluent |
光催化剂材料纳米二氧化钛(P25)购自德国赢创Degussa公司, 纳米三氧化钨购自上海麦克林生化科技有限公司, 纳米氧化锌和纳米三氧化二铁购自阿拉丁试剂(上海)有限公司, g-C3N4由尿素煅烧制备.30% H2O2溶液(分析纯)购自现代东方(北京)科技发展有限公司, 试验用超纯水由Milli-Q(Millipore, 美国)制备.
2.2 实验方法 2.2.1 小试试验取150 mL原水于250 mL的玻璃反应器中, 加入特定浓度(0~1.5 g·L-1)的光催化剂, 将混合溶液超声3 min, 随后在避光条件下以700 r·min-1的转速搅拌30 min, 使体系达到吸附平衡, 在光照前向体系中加入特定浓度(0~400 mg·L-1)的过氧化氢.所用光源为500 W的汞灯(CEL-M500, 北京中教金源), 调节光电流为10 A, 平均光强为0.4 mW·cm-2.将反应器置于光源正下方的磁力搅拌器上, 以700 r·min-1的转速搅拌40 min, 并通过冷凝水维持体系温度恒定.
2.2.2 连续动态试验在小试试验的基础上设计了中试规模的一体化光催化反应装置(图 1), 该装置主要由进水箱、加药箱、光催化组件和出水箱组成.原水与投加药剂混合后经提升泵输送至光催化组件, 经光催化处理后输送至出水端.光催化组件是该装置最重要的部件, 由4个套管式反应器串联组成, 总有效反应容积为1.25 L, 反应停留时间通过进水流量泵进行调节.每个套管反应器的芯管为紫外灯管, 其长度为50 cm, 功率为40 W, 主波长为365 nm;外套管为不锈钢外壳, 内径为57 mm;中间层为石英玻璃, 用于保护灯管, 同时不影响紫外光的传输.水流从石英玻璃与不锈钢外壳之间的环形空腔流过, 其宽度为4 mm.套管式反应器和4 mm极薄液膜层的设计克服了传统反应器光液接触面积小、光强分布不均匀等不足, 能够使光能得到充分的利用.此外, 该装置可以根据不同水样的进出水水质情况通过控制面板来调节紫外灯的启用数量, 减少不必要的能耗.
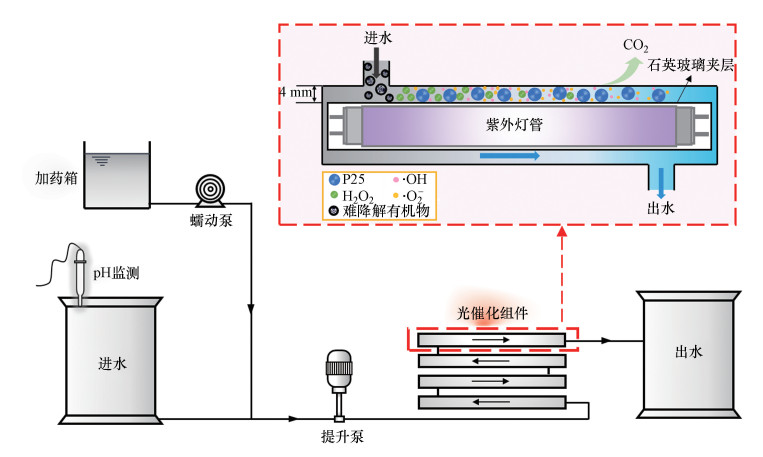 |
| 图 1 一体化光催化装置结构示意图 Fig. 1 Schematic diagram of the photocatalysis pilot plant |
试验开始前, 取5 L原水并加入适量的光催化剂和双氧水, 充分混匀后将混合溶液转移至一体化装置的进水箱中.启动装置, 使装置在黑暗条件下运行30 min, 待混合体系达到吸附平衡并在系统内均匀分散后, 通过控制面板打开紫外光源, 开始光照并计时.装置运行过程中, 每隔一定的时间在出水箱中取50 mL左右的水样, 用于后续分析检测.
2.3 分析方法常规检测项目的测定:样品检测之前, 均经过0.45 μm PES滤膜过滤.化学需氧量(COD)采用哈希(美国)试剂测定, 对于含有H2O2的体系, 样品在检测前应先加入少量的过氧化氢酶以消除样品中残余的H2O2, 避免其对COD测定产生干扰.总有机碳(TOC)和总氮(TN)采用总有机碳分析仪(TOC-L, 日本Shimadzu)测定, UV254采用紫外-可见分光光度计(U-3900, 日本Hitachi)测定, 硝态氮采用离子色谱仪(ICS-5000, 美国Thermo)测定, 氨氮浓度采用纳氏试剂分光光度法(HJ 535-2009)测定, 将总氮与硝态氮及氨氮相减得到有机氮浓度, 生物急性毒性采用斑马鱼卵法(HJ 1069-2019)测定.
自由基浓度的测定:采用电子顺磁共振(EPR)结合自旋捕获的方法测定体系中的自由基浓度.分别以超纯水和二甲基亚砜为溶剂, 向反应体系中加入100 mmol·L-1的自由基捕获剂DMPO(5, 5-二甲基-1-吡咯啉-1-邻二甲苯), 利用电子顺磁共振波谱仪(A300, 德国Bruker)检测羟基自由基(·OH)和超氧阴离子自由基(·O2-).
傅里叶变换红外光谱(FT-IR)分析:采用傅里叶红外变换光谱仪(Nicolet iS50, 美国Thermo)对样品中有机物的官能团进行分析.对于样品的制备, 首先将350 mL的水样置于-80 ℃超低温冰箱中冷冻, 使其凝固形成冰块, 随后放入真空冷冻干燥机中进行干燥.将10 mg干燥后的样品与990 mg KBr混匀并碾磨压片, 光谱扫描范围为4000 ~ 400 cm-1.
凝胶渗透色谱(GPC)分析:采用凝胶渗透色谱仪(Breeze 2, 美国Waters)对样品中有机物的相对分子质量分布进行分析.色谱柱为HSPgel AQ3.0凝胶色谱柱(6.0 mm×150 mm), 流动相为0.1 mol·L-1的NaCl水溶液, 流速为0.3 mL·min-1, 进样体积为20 μL, 柱温为30 ℃.采用紫外检测器, 检测波长设置为254 nm.
三维荧光光谱(EEM)分析:采用荧光分光光度计(F-7000, 日本Hitachi)对样品中有机物的种类进行分析.激发波长范围为200~450 nm, 发射波长范围为280~550 nm, 扫描间隔为5 nm.
3 结果与讨论(Results and discussion) 3.1 光芬顿深度处理条件优化针对制药废水二级出水, 分别研究了光催化剂种类、光催化剂投加量、过氧化氢投加量对处理效果的影响, 并对比了UV/TiO2、UV/H2O2、UV/TiO2/H2O2 3种反应体系的处理效果, 结果如图 2所示.
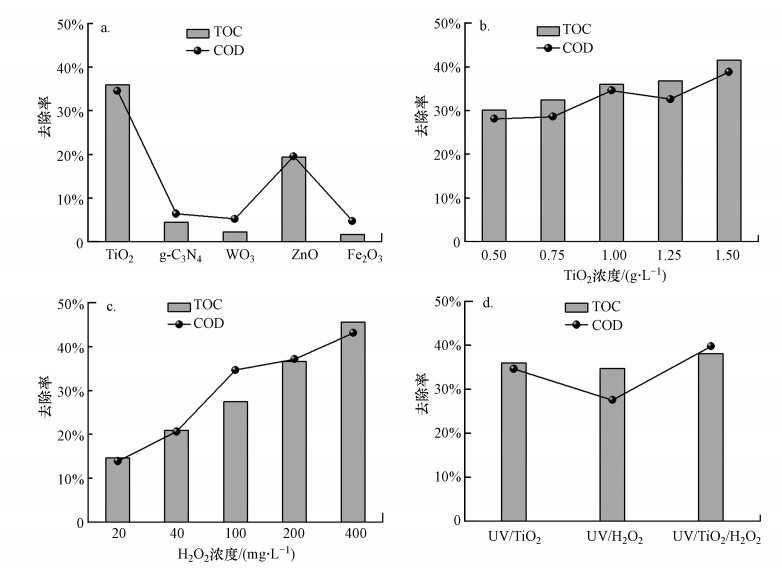 |
| 图 2 不同反应体系在光照40 min后的COD和TOC去除率 (a.不同催化剂的影响, b.不同TiO2浓度的影响, c.不同H2O2浓度的影响, d.不同UV/TiO2/H2O2体系) Fig. 2 Removal efficiency of COD and TOC after 40 min UV irradiation in different reaction systems |
为了筛选合适的催化剂, 通过小试试验研究了5种常用的光催化剂对制药废水二级出水的COD和TOC去除效率, 催化剂投加量均为1 g·L-1, 光照时间为40 min.光照前, 首先将混合体系在避光条件下搅拌30 min, 实验结果表明, 在无UV光照的情况, 催化剂对有机物的降解基本不发挥作用, 暗处理30 min后溶液TOC的变化在1 mg·L-1范围内, 可忽略不计.如图 2a所示, 在TiO2、ZnO、WO3、Fe2O3、g-C3N4 5种光催化剂中, TiO2对制药废水二级出水的催化降解效果最好, 光照40 min后COD和TOC的去除率分别达到34.6%和36.0%, 远高于其他光催化剂.研究表明, 纳米TiO2具有很高的光催化活性, 能够有效去除多种污染物(Al-Mamun et al., 2019).此外, 纳米TiO2还具有化学稳定性高、无毒无害、价格低廉等优点, 已被广泛应用于光催化相关研究中(Das et al., 2014;Reina et al., 2019).综合上述分析, 选择TiO2作为连续动态试验的光催化剂.
在此基础上, 进一步研究TiO2投加量对制药废水二级出水催化降解效果的影响.由图 2b可知, 当TiO2投加量为0.5~1.0 g·L-1时, COD去除率随光催化剂投加量增加而逐渐升高, 当TiO2投加量进一步提高到1.5 g·L-1时, COD去除率的变化较小甚至略有下降.在一定范围内增大TiO2的投加量可以增加催化剂的活性位点, 促进自由基的产生, 从而提高有机污染物的降解效率.然而, 过高的投加量会造成光散射, 并增大溶液的浊度, 导致光吸收效率下降, 从而影响催化降解效果(Tsai et al., 2009;Chen et al., 2016).综合上述分析, 确定TiO2的投加量为1 g·L-1.
对于UV/H2O2体系, 研究了不同H2O2投加量对二级出水COD和TOC的去除效果.由图 2c可知, 随着H2O2投加量的增加, COD和TOC的去除率也持续升高.当H2O2投加量为20~100 mg·L-1时, COD和TOC去除率显著增长, 在H2O2投加量为100 mg·L-1时分别达到27.5%和34.7%;当投加量进一步增大到100~400 mg·L-1时, COD和TOC去除率的增长则相对较缓.研究表明, 在一定范围内, H2O2投加量与体系内自由基产生量正相关, 而当投加量超过一定范围时, 过量的H2O2会因自淬灭作用对降解效率造成抑制(Wols et al., 2015).综合考虑处理效果及经济成本等因素, 最终确定H2O2投加量为100 mg·L-1.
基于上述结果, 在最佳反应条件下(TiO2投加量为1 g·L-1, H2O2投加量为100 mg·L-1), 进一步对比了UV/TiO2、UV/H2O2、UV/TiO2/H2O2 3种AOPs工艺对制药废水二级出水的处理效果.如图 2d所示, 光照40 min后, UV/TiO2/H2O2体系的COD和TOC去除率分别达到39.7%和38.1%, 高于UV/TiO2和UV/H2O2体系, 这表明TiO2和H2O2之间可能存在协同增效作用.综合上述分析, 本研究的连续动态试验拟采用UV/TiO2/H2O2反应体系处理制药废水二级出水, 其中, 光催化剂投加量为1 g·L-1的TiO2, H2O2投加量为100 mg·L-1.
3.2 UV/TiO2/H2O2体系机理研究为了进一步明确UV/TiO2/H2O2体系去除有机污染物的机理, 利用电子顺磁共振结合自旋捕获的方法, 检测体系中的自由基, 结果如图 3a和3b所示.本研究采用的自由基捕获剂DMPO会与·OH和·O2-反应, 分别生成相对稳定的自旋加合物DMPO-OH和DMPO-OOH.图 3a的EPR波谱由4条谱线组成, 强度比为1∶2∶2∶1, 属于典型的DMPO-OH图谱(赵保路, 2010), 表明体系中有·OH的存在.由图 3a可知, UV/TiO2/H2O2体系中DMPO-OH特征峰强度明显高于UV/TiO2和UV/H2O2体系, 说明UV/TiO2/H2O2体系中·OH的产生量更高, 也表明H2O2的引入对·OH的产生起到了促进作用.同样, 由图 3b可知, 反应体系中有·O2-产生, 且UV/TiO2/H2O2体系中·O2-的产生量也明显高于UV/TiO2和UV/H2O2体系.该研究结果表明, TiO2和H2O2共存能够促进体系中羟基自由基和超氧阴离子自由基的生成, 从而提高UV/TiO2/H2O2体系的催化降解效率.
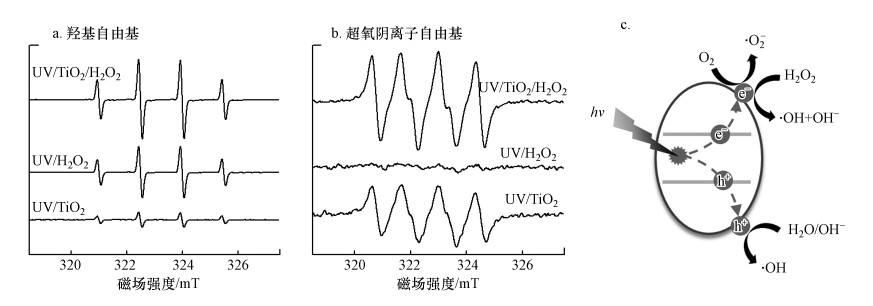 |
| 图 3 不同反应体系的EPR谱图(a、b)及UV/TiO2/H2O2体系的反应机理(c) Fig. 3 EPR spectra obtained in different reaction systems (a, b) and the mechanism of UV/TiO2/H2O2 system (c) |
EPR分析结果表明, 在UV/TiO2/H2O2体系中, TiO2和H2O2具有协同增效作用, 推测其主要反应机理如图 3c所示.在入射光的激发下, H2O2快速分解, 促进·OH的产生, 而·OH具有强氧化活性, 能够高效地去除有机污染物;同时, H2O2能够捕获TiO2导带上的电子, 减少电子与空穴的复合, 从而提高光量子效率;此外, H2O2分解生成的H2O和O2分子也有助于·OH和·O2-的产生(Li et al., 2016).
3.3 一体化光催化装置运行效果 3.3.1 二级出水处理效果基于3.1节的条件优化结果(光催化剂TiO2投加量为1 g·L-1, H2O2投加量为100 mg·L-1), 进一步利用一体化光催化装置研究了UV/TiO2/H2O2光芬顿工艺对制药废水二级出水的处理效果, 运行过程中COD、TOC、UV254和TN等水质参数的变化情况如图 4所示.随着光芬顿反应的进行, COD、TOC、UV254和TN均呈现出明显降低的趋势, 并在光照时间达到30~45 min后稳定在较低水平.其中, COD在30 min内即可降至20 mg·L-1(图 4a), 去除率超过50%, 完全可以达到国家和地方制定的制药废水排放标准.UV254常用于表征样品中芳香族化合物的含量, 而SUVA(UV254与DOC的比值)则被广泛用于表征有机物的不饱和程度(金鑫等, 2015).由图 4b可以看出, 随着光照时间的延长, UV254和SUVA值呈现出下降的趋势, 表明光芬顿反应能够分解废水中的芳香族化合物和不饱和化合物, 降低废水的芳香度和不饱和度.此外, 由图 4c可知, 光芬顿反应能够有效促进氮素的去除和转化, 总氮明显降低, 有机氮逐渐转化为无机氮.该研究结果表明, 本研究自主设计的一体化光催化装置能够利用光芬顿技术快速高效地降解制药废水二级出水中的有机污染物.
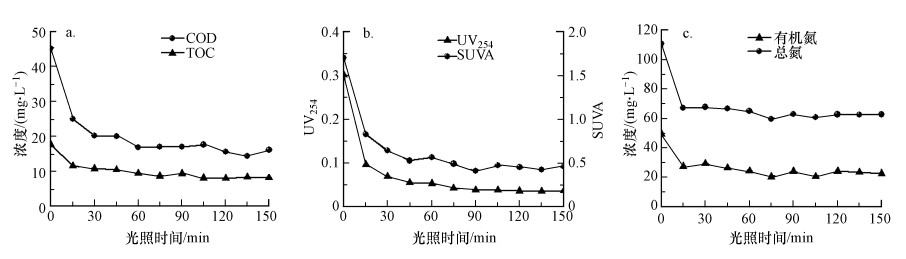 |
| 图 4 一体化装置运行过程中水样的有机物浓度(a)、吸光度(b)、氮浓度(c)随光照时间的变化 Fig. 4 Time-dependent changes of organics concentration (a), absorbance (b) and nitrogen concentration (c) during operation of the integrated reactor |
为了进一步探究光芬顿处理前后有机物的组成和特性的变化规律, 对不同时间的出水进行凝胶渗透色谱和傅里叶变换红外光谱的分析测试.
如图 5a所示, 该制药废水二级出水的GPC谱图中主要有两个信号峰, 分别代表大分子化合物(峰A)和小分子化合物(峰B).整体上看, 峰A和峰B的强度均呈现出随处理时间降低的趋势, 但相比于峰B, 峰A的下降幅度更大, 说明在光芬顿反应过程中大分子化合物比小分子化合物更易于降解.此外, 随着反应的持续进行, 峰B逐渐取代峰A成为最主要的信号峰, 这表明光芬顿处理过程将大量的大分子化合物分解成小分子, 而小分子化合物的去除率相对较低, 因此, 处理后水样的组成以小分子化合物为主.
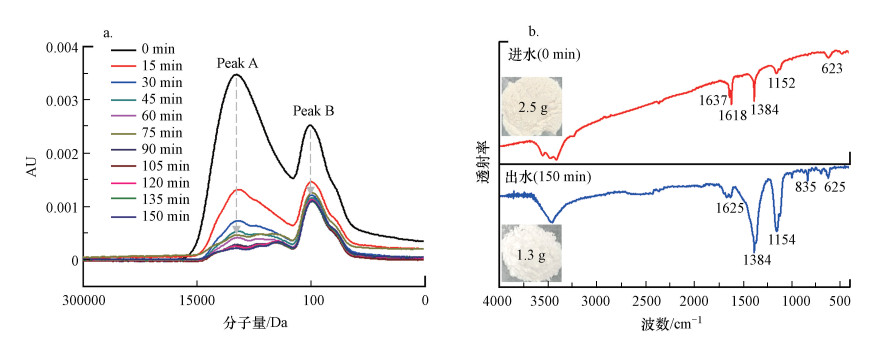 |
| 图 5 不同时间水样的凝胶色谱图(a)和傅里叶变换红外光谱图(b) Fig. 5 GPC spectra (a) and FT-IR spectra (b) of the water samples obtained at different intervals |
对同等体积(350 mL)的进水(光芬顿处理前)和出水(光芬顿处理后)水样进行干燥(详见2.3节), 分别得到2.5 g和1.3 g粉末, 且前者呈淡黄色, 而后者呈白色(图 5b).结合3.3.1节的结果可知, 粉末样品质量减少及颜色变浅可能是因为光芬顿处理去除了二级出水中的部分有机物和色度, 这与COD和UV254的减小是相符的.如图 5b所示, 进水和出水的FT-IR光谱的特征峰数量及位置基本相同.波数1500~1690 cm-1范围内主要是碳碳双键、碳氮双键等双键伸缩振动区, 也包括苯环骨架等不饱和结构;波数1384 cm-1附近主要是甲基等饱和烃基;波数小于1000 cm-1的吸收峰则可能是苯环上的取代基(王佳琴等, 2018).对比进水和出水的FT-IR光谱可以看出, 出水中1384 cm-1处的吸收峰信号有所增强, 而1625 cm-1处的峰强相对较弱.峰强的相对变化可能是由于光芬顿处理过程氧化降解了部分不饱和化合物, 使样品中不饱和结构减少, 饱和烃基增多, 与SUVA的变化趋势一致.
不同时间出水的三维荧光光谱如图 6所示.根据Chen等(2015)的研究, 可将EEM光谱划分为5个区域, 各区域的波长范围及主要有机物类型见表 2.由图 6可知, 原水中的荧光物质主要位于区域Ⅳ和区域Ⅴ, 说明该制药废水二级出水中的溶解性有机物(DOM)主要为微生物产物和腐殖酸类物质.经过光芬顿处理后, EEM光谱中各荧光峰的峰强显著降低、峰形迅速变小, 整体上各类有机污染物都得到了有效的去除.光照15 min后, 区域Ⅴ的荧光信号几乎完全消失, 说明腐殖酸类物质在光芬顿作用下芳香环、共轭键减少, 腐殖化程度显著降低.
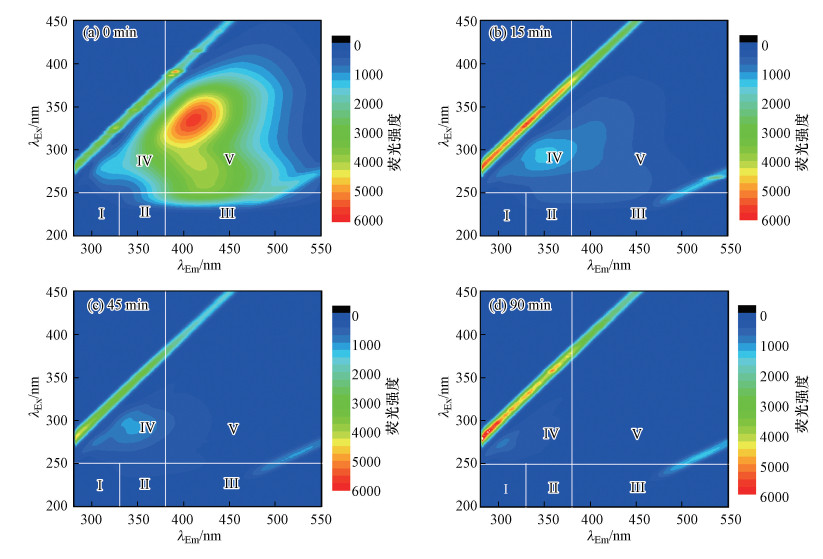 |
| 图 6 不同时间水样的三维荧光光谱图 Fig. 6 EEM spectra of the water samples obtained at different intervals |
| 表 2 各荧光区域的波长范围及有机物类型 Table 2 Wavelength boundaries and representative substance of different fluorescence regions |
选择斑马鱼为研究材料, 将斑马鱼胚胎分别暴露于制药废水二级出水(对照组)及深度处理出水(实验组)中, 观察斑马鱼胚胎的形态改变, 结果见图 7a~7f.如图所示, 对照组的斑马鱼胚胎, 在暴露时间24 h时体节未形成(图 7a), 48 h时出现卵凝结现象(图 7b), 72 h时卵黄囊水肿(图 7c);而实验组的胚胎发育正常(图 7d~7f), 未观察到畸形发育现象.
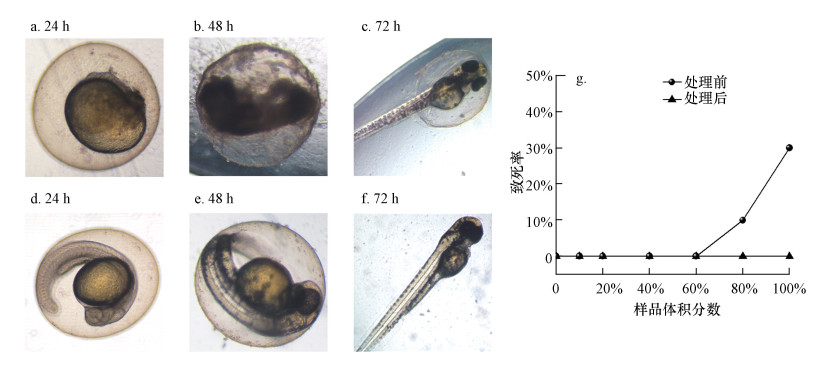 |
| 图 7 光芬顿深度处理前(a~c)和处理后(d~f)的制药废水对斑马鱼胚胎发育及孵化率(g)的影响 Fig. 7 Effect of the wastewater before (a~c) and after (d~f) UV/TiO2/H2O2 on zebrafish embryo development and hatchability (g) |
在斑马鱼胚胎发育过程中, 卵凝结、体节未形成、尾部未分离等畸形现象会导致胚胎发育停止, 胚胎趋于死亡或已经死亡, 可作为鱼卵镜检的测试终点.按照一定比例对水样进行稀释, 对不同稀释倍数的水样引起的斑马鱼胚胎致死效应进行统计, 结果见图 7g.如图所示, 深度处理前的制药废水二级出水对胚胎的致死效应随其浓度的增大而增强.当二级出水的体积分数低于40%时, 胚胎致死率为0, 与实验组没有显著差异;当二级出水的体积分数高于60%时, 胚胎致死率急增, 对于未经稀释的二级出水, 胚胎致死率可达30%, 而实验组的致死率依然为0.
上述研究结果表明, 该制药废水二级出水对斑马鱼胚胎的孵化和发育存在一定的毒性效应, 而光芬顿深度处理能够显著降低其生物毒性, 经过深度处理后该废水对斑马鱼胚胎发育基本不存在毒性效应.制药废水成分复杂, 含有大量有机污染物, 其中, 卤素化合物、硝基化合物、有机氮化合物等难降解污染物不仅对微生物的活性有抑制作用, 同时还使废水产生了较高的生物毒性(邓睿, 2013;Shi et al., 2017).光芬顿高级氧化技术可以通过产生自由基, 无选择性地去除制药废水中的难降解有机物, 使废水中的有机碳和有机氮含量下降(图 4), 从而降低其生物毒性.
4 结论(Conclusions)1) 在UV/TiO2、UV/ H2O2、UV/TiO2/H2O2 3种反应体系中, UV/TiO2/H2O2光芬顿反应体系对制药废水二级出水的催化降解效果最好.其中, TiO2最佳投加量为1 g·L-1, H2O2最佳投加量为100 mg·L-1.
2) 一体化光催化装置能够利用UV/TiO2/H2O2光芬顿技术快速高效地降解该二级出水中的有机污染物, 光照30~45 min后COD、TOC等指标均降低至较低水平, COD去除率达到50%以上.
3) UV/TiO2/H2O2深度处理会改变该制药废水的有机物特性及生物毒性, 表现为:大分子有机物被分解小分子, 小分子有机物的含量相对增加;不饱和结构减少, 饱和烃基增多;主要的DOM组分微生物产物和腐殖质, 经处理后基本降解完全;废水生物毒性经深度处理后显著降低, 对斑马鱼胚胎无致畸致死效应.
Al-Mamun M R, Kader S, Islam M S, et al. 2019. Photocatalytic activity improvement and application of UV-TiO2 photocatalysis in textile wastewater treatment: a review[J]. Journal of Environmental Chemical Engineering, 7(5): 103248. DOI:10.1016/j.jece.2019.103248 |
Bai X, Lyu L, Ma W, et al. 2016. Heterogeneous UV/Fenton degradation of bisphenol A catalyzed by synergistic effects of FeCo2O4/TiO2/GO[J]. Environmental Science & Pollution Research International, 23(22): 1-10. |
Chen W, Westerhoff P, Leenheer J A, et al. 2015. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 37(24): 5701-5710. |
Chen Y, Liu K R. 2016. Preparation and characterization of nitrogen-doped TiO2/diatomite integrated photocatalytic pellet for the adsorption-degradation of tetracycline hydrochloride using visible light[J]. Chemical Engineering Journal, 302(15): 682-696. |
Chew C M, Aroua M K, Hussain M A. 2018. Advanced process control for ultrafiltration membrane water treatment system[J]. Journal of Cleaner Production, 179: 63-80. DOI:10.1016/j.jclepro.2018.01.075 |
Cimbritz M, Edefell E, Thörnqvist E, et al. 2019. PAC dosing to an MBBR-Effects on adsorption of micropollutants, nitrification and microbial community[J]. Science of the Total Environment, 677: 571-579. DOI:10.1016/j.scitotenv.2019.04.261 |
Das R, Sarkar S, Chakraborty S, et al. 2014. Remediation of antiseptic components in wastewater by photocatalysis using TiO2 nanoparticles[J]. Industrial & Engineering Chemistry Research, 53(8): 3012-3020. |
邓睿. 2013. 制药废水深度处理研究[D]. 广州: 华南理工大学
|
Fan D, Ding L, Huang H, et al. 2017. Fluidized-bed Fenton coupled with ceramic membrane separation for advanced treatment of flax wastewater[J]. Journal of Hazardous Materials, 340: 390-398. DOI:10.1016/j.jhazmat.2017.05.055 |
Gadipelly C, Pérez-González Antía, Yadav G D, et al. 2014. Pharmaceutical industry wastewater: review of the technologies for water treatment and reuse[J]. Industrial & Engineering Chemistry Research, 53(29): 11571-11592. |
Guan R P, Yuan X Z, Wu Z B, et al. 2018. Principle and application of hydrogen peroxide based advanced oxidation processes in activated sludge treatment: A review[J]. Chemical Engineering Journal, 339: 519-530. DOI:10.1016/j.cej.2018.01.153 |
Hansen K M S, Spiliotopoulou A, Chhetri R K, et al. 2016. Ozonation for source treatment of pharmaceuticals in hospital wastewater-ozone lifetime and required ozone dose[J]. Chemical Engineering Journal, 290: 507-514. DOI:10.1016/j.cej.2016.01.027 |
Jain B, Singh A K, Kim H, et al. 2018. Treatment of organic pollutants by homogeneous and heterogeneous Fenton reaction processes[J]. Environmental Chemistry Letters, 16: 947-967. DOI:10.1007/s10311-018-0738-3 |
金鑫, 金鹏康, 孔茜, 等. 2015. 污水厂二级出水溶解性有机物臭氧化特性研究[J]. 中国环境科学, 35(10): 2985-2990. DOI:10.3969/j.issn.1000-6923.2015.10.014 |
Li W Y, Liu Y, Sun X L, et al. 2016. Photocatalytic degradation of MC-LR in water by the UV/TiO2/H2O2 process[J]. Water Science & Technology Water Supply, 16(1): 34-43. |
Li Z, Mclachlan M S. 2019. Biodegradation of chemicals in unspiked surface waters downstream of wastewater treatment plants[J]. Environmental Science and Technology, 53(4): 1884-1892. DOI:10.1021/acs.est.8b05191 |
Mano T, Nishimoto S, Kameshima Y, et al. 2015. Water treatment efficacy of various metal oxide semiconductors for photocatalytic ozonation under UV and visible light irradiation[J]. Chemical Engineering Journal, 264: 221-229. DOI:10.1016/j.cej.2014.11.088 |
Qanbarzadeh M, Wang D, Ateia M, et al. 2021. Impacts of reactor configuration, degradation mechanisms, and water matrices on perfluorocarboxylic acid treatment efficiency by the UV/Bi3O(OH)(PO4)2 photocatalytic process[J]. ACS Est Engg, 1: 239-248. DOI:10.1021/acsestengg.0c00086 |
Reina A C, Piernas A B M, Bertakis Y, et al. 2019. TiO2 photocatalysis under natural solar radiation for the degradation of the carbapenem antibiotics imipenem and meropenem in aqueous solutions at pilot plant scale[J]. Water Research, 166: 115037. DOI:10.1016/j.watres.2019.115037 |
Rott E, Minke R, Bali U, et al. 2017. Removal of phosphonates from industrial wastewater with UV/FeII, Fenton and UV/Fenton treatment[J]. Water Research, 122: 345-354. DOI:10.1016/j.watres.2017.06.009 |
Sengul A B, Ersan G, Tufekci N. 2017. Removal of intra- and extracellular microcystin by submerged ultrafiltration (UF) membrane combined with coagulation/flocculation and powdered activated carbon (PAC) adsorption[J]. Journal of Hazardous Materials, 343: 29-35. |
Shi X, Leong K Y, Ng H Y. 2017. Anaerobic treatment of pharmaceutical wastewater: A critical review[J]. Bioresource Technology, 245: 1238-1244. DOI:10.1016/j.biortech.2017.08.150 |
Silva J R O, Santos D S, Santos U R, et al. 2017. Electrochemical and/or microbiological treatment of pyrolysis wastewater[J]. Chemosphere, 185: 45-151. |
Tsai W T, Lee M K, Su T Y, et al. 2009. Photodegradation of bisphenol-A in a batch TiO2 suspension reactor[J]. Journal of Hazardous Materials, 168(1): 269-275. DOI:10.1016/j.jhazmat.2009.02.034 |
王佳琴, 李卫华, 申慧彦, 等. 2018. 污水厂进出水中DOM的三维荧光和FTIR光谱解析简[J]. 环境科学与技术, (1): 71-76. |
Wols B A, Harmsen D J H, Beerendonk E F, et al. 2015. Predicting pharmaceutical degradation by UV(MP)/H2O2 processes: A kinetic mode[J]. Chemical Engineering Journal, 263: 336-345. DOI:10.1016/j.cej.2014.10.101 |
Xiao J, Xie Y, Cao H. 2015. Organic pollutants removal in wastewater by heterogeneous photocatalytic ozonation[J]. Chemosphere, 121: 1-17. |
袁宏林, 郝丽伟, 马晓妍, 等. 2019. UV/TiO2光催化过程对二级处理出水多重生物效应的削减特性研究[J]. 环境科学学报, 39(8): 2499-2507. |
赵保路. 2010. 电子自旋共振(ESR)技术在生物和医学中的应用[J]. 波谱学杂志, 27(1): 51-67. |
 2021, Vol. 41
2021, Vol. 41


