2. 广东省大气环境与污染控制重点实验室, 广州 510006;
3. 挥发性有机物污染治理技术与装备国家工程实验室, 广州 510006
2. Guangdong Provincial Key Laboratory of Atmospheric Environment and Pollution Control, Guangzhou 510006;
3. National Engineering Laboratory for VOCs Pollution Control Technology and Equipment, Guangzhou 510006
挥发性有机化合物(VOCs)对生态环境和人类健康的严重危害已引起全世界的关注.同时, 为了实施我国碳达峰行动方案, 切实有效地控制工业源VOCs排放, 工业涂装、石油化工、包装印刷等行业及燃煤电厂已经开始了以水溶性VOCs酯类溶剂替代传统苯系物溶剂的环保化进程(Zheng et al., 2013; 谢轶嵩等, 2018; 赵锐等, 2018; Li et al., 2019), 其中, 以乙酸乙酯为代表的水溶性溶剂备受青睐(Wang et al., 2014; 田亮等, 2017).但大量乙酸乙酯的排放不仅会对环境造成污染, 而且会危害人体健康, 高浓度吸入可引起麻醉作用, 导致急性肺水肿, 以及肝、肾损害等(Shen et al., 2018; 翟增秀等, 2018).为了减少和避免其对环境的潜在污染, 有必要对乙酸乙酯进行回收处理.在许多可用于VOCs处理的技术中, 吸附法因具有吸附装置简单、运行成本低和能耗低等特点, 成为可靠的VOCs去除方法.在吸附剂的选取中, NaY沸石因具有良好的水热稳定性、高比表面积、丰富的微孔结构和对不同VOCs良好的吸附性能等特点而被广泛用于吸附处理中(Larsen, 2007).
燃煤电厂煤燃烧产生的固体废物粉煤灰因含有大量硅、铝元素, 可用作NaY沸石合成的原材料.据统计, 2019年, 我国重点工业企业的粉煤灰产生量为5.4亿t, 综合利用量为4.1亿t.在碳中和背景下, 实现减量化同时提升经济性是发展的必然趋势(赵书言, 2021).因此, 研究一种节约能源的合成方法用于制备粉煤灰源NaY沸石, 再将其应用于燃煤电厂废气吸附处理中, 从而实现废物再利用具有重要意义.
NaY沸石具有较大的比表面积和丰富的微孔结构, 对不同VOCs具有良好的吸附性能(Zhang et al., 2012; Nigar et al., 2015).然而, 利用粉煤灰合成NaY沸石的研究报道还相对较少, 例如, Zhou等(2012)通过添加其他原料(如氢氧化铝)来调整Si/Al比, 制备了NaY沸石;还有一些研究通过长时间的水热结晶(17~96 h)和控制温度(90~120 ℃), 合成了具有低比表面积的NaY沸石(133.85 m2·g-1)(Carlos et al., 2012; Padhy et al., 2015; Ren et al., 2020).此外, 目前NaY沸石的合成往往需要有机模板(He et al., 2016; Qamar et al., 2016; Zhao et al., 2016), 不利于环境友好发展(Mu et al., 2019).总体而言, 目前采用粉煤灰所制备的NaY沸石比表面积较低且缺乏多级孔结构(Carlos et al., 2012).
基于此, 本研究主要探索碱熔融-水热结晶法合成粉煤灰源高比表面积NaY沸石的最佳条件, 考察不同Si/Al比的粉煤灰、结晶温度、结晶时间和碱浓度4个因素对合成高比表面积NaY沸石的影响, 同时还使用动态吸附评价装置研究粉煤灰源NaY沸石对乙酸乙酯的吸附性能.
2 材料与方法(Experimental) 2.1 实验原料粉煤灰1号和2号分别取自河南大唐燃煤电厂两个批次的粉煤灰, 粉煤灰3号取自湖南衡阳燃煤电厂, 分别标记为CFA-1、CFA-2、CFA-3;盐酸购自广州东征化玻有限公司;氢氧化钠购自上海阿拉丁生化科技股份有限公司;去离子水.
2.2 实验与分析设备马弗炉(广州市红图仪器有限公司);气相色谱仪(GC9790-Ⅱ, 福立仪器);X射线粉末衍射仪(D8 Advance, 德国布鲁克公司);氮气物理吸附仪(ASAP-2020 V4.03, 美国麦克公司);电感耦合等离子体发射光谱(Agilent ICPOES730, 美国安捷伦公司);X-射线荧光衍射分析(ARLAdvantX IntellipowerTM3600, 美国赛默飞);吸附评价反应装置(自制).
2.3 粉煤灰源沸石制备方法 2.3.1 粉煤灰预处理粉煤灰与盐酸溶液按照1 g∶10 mL的比例进行混合, 80 ℃油浴搅拌2 h, 然后用去离子水洗至中性, 烘干.该步骤主要去除粉煤灰中Fe、K、Cr等金属微量元素.酸浸后的粉煤灰1、粉煤灰2、粉煤灰3分别标记为Al-CFA-1、Al-CFA-2、Al-CFA-3.
2.3.2 碱熔煅烧方法将盐酸处理后的粉煤灰与氢氧化钠按照1 g∶1.2 g的比例进行研磨, 然后放入马弗炉中于550 ℃下煅烧1.5 h, 活化粉煤灰中的Si和Al元素生成Na2SiO3和霞石(NaAlSiO4).
2.3.3 老化将碱熔融后的粉煤灰、氢氧化钠和去离子水按照1 g∶(0.3、0.4、0.5、0.6 g)∶5 mL的比例进行混合, 在室温下搅拌12 h进行老化.
2.3.4 水热合成沸石方法将老化的混合液倒入100 mL聚四氟乙烯内衬中, 再放入反应釜中密封, 然后转移至烘箱中在适当的温度(45、65、85和105 ℃)和时间(6、8、10及12 h)下分别合成沸石;反应完成后, 冷却至室温, 将里面的样品洗涤至中性, 烘干即得到沸石样品.
3 结果与讨论(Results and analysis) 3.1 不同硅铝比粉煤灰制备的NaY沸石对比与分析因NaY沸石的硅铝比(Si/Al)在2左右, 所以选取Si/Al比在1~2左右的粉煤灰用于制备NaY沸石.根据ICP-OES测试结果(表 1), CFA-1、CFA-2和CFA-3的Si/Al比分别为2.28、1.94和1.16.如图 1所示, 虽然3种粉煤灰的Si/Al比不同, 但其均在碱浓度为2 mol·L-1、温度为65 ℃的条件下水热结晶12 h后生成了NaY沸石, 但CFA-3合成的晶相中既有NaY沸石又有NaA沸石, 说明Si/Al比为2左右的粉煤灰更适合合成NaY沸石.
| 表 1 3种粉煤灰CFA-1、CFA-2和CFA-3的硅、铝含量和硅铝比 Table 1 Si, Al contents and Si/Al ratios of three kinds of coal fly ash CFA-1, CFA-2 and CFA-3 |
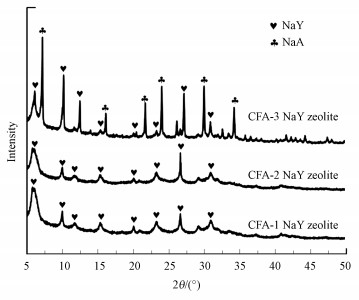 |
| 图 1 3种粉煤灰制备的NaY沸石的XRD图 Fig. 1 XRD patterns of NaY zeolite prepared by three kinds of coal fly ash |
由表 2和图 2可知, 合成的NaY沸石的比表面积及孔容均有较大提升, CFA-1源、CFA-2源、CFA-3源NaY沸石的比表面积分别由CFA-1、CFA-2、CFA-3的28.74、25.30、41.58 m2·g-1提升到654.86、630.25、265.47 m2·g-1.这些结果证明Si/Al比在2左右的粉煤灰用于合成高比表面积的NaY沸石更合适.
| 表 2 3种NaY沸石的比表面积及孔容分析 Table 2 Analysis of specific surface area and pore volume of three NaY zeolites |
 |
| 图 2 3种NaY分子筛的N2吸附/脱附等温线及孔径分布 Fig. 2 N2 adsorption/desorption isotherms and pore-size distributions of three NaY zeolites |
水热结晶温度是影响沸石合成最重要的因素之一.不同的研究给出了粉煤灰合成NaY沸石的不同水热结晶温度, 本实验采用3种粉煤灰分别在45、65、85和105 ℃下进行水热合成(碱浓度2 mol·L-1, 时间12 h), 筛选出最佳的结晶温度, 分别命名为CFAZ-x-Yy (x代表 1、2、3号粉煤灰, y代表合成沸石的温度).如图 3所示, 3种粉煤灰在65 ℃下水热合成的沸石与标准NaY沸石的XRD峰更相符.
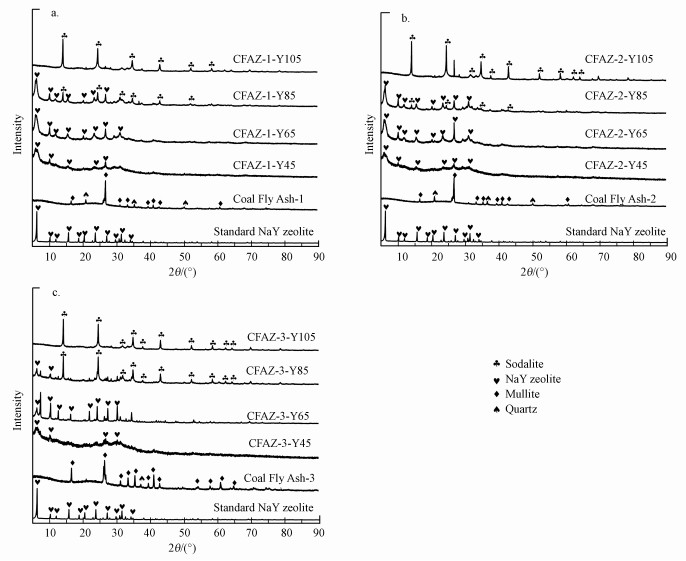 |
| 图 3 标准NaY沸石、3种粉煤灰及其在不同温度下合成的沸石的XRD图 Fig. 3 XRD patterns of standard NaY zeolite, three kinds of coal fly ash and zeolite synthesized at different temperature from three coal fly ash |
合成的NaY沸石(CFAZ-1-Y65和CFAZ-2-Y65)具有最大的比表面积654.86 m2·g-1和630.25 m2·g-1 (表 3和图 4), 接近于表 3中列出的标准NaY沸石的比表面积683.78 m2·g-1;温度升高到85 ℃时, 开始出现方钠石, 比表面积也分别降至410.65 m2·g-1和445.17 m2·g-1;当温度升高到105 ℃时, 比表面积降至最低, 分别为47.07 m2·g-1和25.58 m2·g-1, 甚至几乎等同于酸化处理后的粉煤灰的比表面积.
| 表 3 3种粉煤灰在不同温度下合成的NaY沸石的比表面积及孔容分析 Table 3 Analysis of specific surface areas and pore volumes of NaY zeolites synthesized by three kinds of coal fly ash at different temperatures |
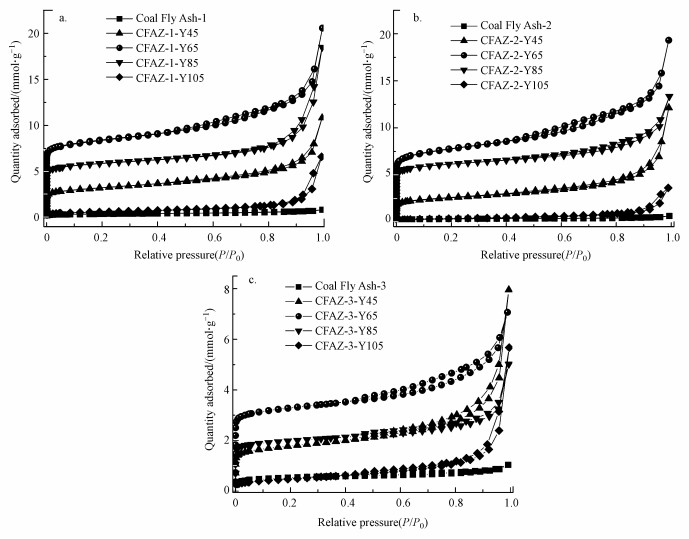 |
| 图 4 不同温度下3种粉煤灰及合成样品的氮气吸脱附曲线 (a.CFA-1, b.CFA-2, c.CFA-3) Fig. 4 Nitrogen adsorption-desorption curves of three fly ashes and their samples synthesized at different temperatures (a.CFA-1, b.CFA-2, c.CFA-3) |
在65 ℃的水热处理下合成的NaY沸石具有最高的比表面积, 这是由于65 ℃更有利于样品在水热结晶过程中脱硅从而形成微孔和中孔(Zhang et al., 2018; 刘思远等, 2019).这与ICP-MS的结果一致, 在65 ℃下合成的NaY沸石的硅含量最少(表 4).
| 表 4 CFA-1、CFA-2、CFA-3及在不同温度下制备的样品的硅、铝含量及其Si/Al比 Table 4 CFA-1, CFA-2, CFA-3 and the silicon and aluminum contents and Si/Al of the samples prepared at different temperatures |
水热结晶过程中, 碱度对NaY沸石的合成具有重要作用, 碱度太低则不会生成沸石, 碱度太高则生成很多杂相.使用Si/Al=1.94的粉煤灰, 在水热温度为65 ℃, 碱浓度分别为1.5、2.0、2.5和3.0 mol·L-1的碱度下结晶12 h, 研究NaY沸石是否成功合成.如图 5所示, 2.0 mol·L-1碱浓度下合成的沸石的结晶情况最好, 而1.5、2.5和3.0 mol·L-1碱浓度下合成的产物有些角度没有产生NaY沸石的特征峰, 所以2.0 mol·L-1碱浓度对合成NaY沸石最有利.
 |
| 图 5 不同碱浓度下合成沸石的物相分析图 Fig. 5 Phase analysis of zeolites synthesized at different alkali concentrations |
如表 5和图 6所示, 随着水热碱浓度的升高, 合成产物的比表面积先升高后降低, 2.0 mol·L-1碱浓度下合成的NaY沸石的比表面积(630.25 m2·g-1)及孔容均最大.
| 表 5 不同水热碱浓度下合成的NaY沸石的比表面积及孔容分析 Table 5 Specific surface areas and pore volumes analysis of NaY zeolites synthesized by coal fly ash at different hydrothermal alkali concentrations |
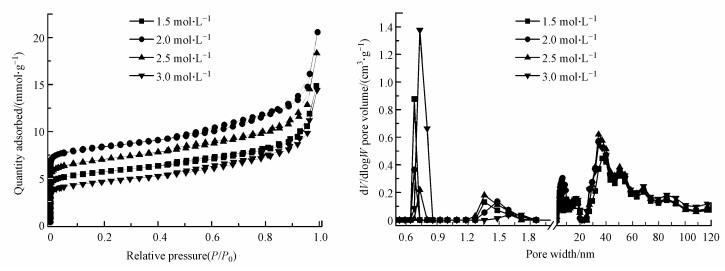 |
| 图 6 不同水热碱浓度下合成的NaY沸石的N2吸附/脱附等温线及孔径分布 Fig. 6 N2 adsorption/desorption isotherms and pore size distribution of NaY zeolites synthesized by coal fly ash at different hydrothermal alkali concentrations |
水热结晶过程中, 时间也对NaY沸石的合成具有一定影响, 水热时间太短则不利于结晶.使用Si/Al=1.94的粉煤灰, 在水热温度为65 ℃, 碱浓度为2.0 mol·L-1的条件下分别结晶6、8、10和12 h, 观察NaY沸石是否结晶完成.如XRD图(图 7)所示, 在6、8、10和12 h的结晶时间下合成沸石的物相均为NaY沸石的特征峰且无明显差别, 所以均可以合成NaY沸石.
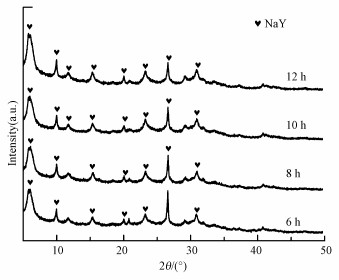 |
| 图 7 粉煤灰在6、8、10及12 h水热结晶后生成的产物的物相分析图 Fig. 7 Phase analysis diagram of products formed by hydrothermal crystallization of fly ash at 6, 8, 10 and 12 h |
如表 6和图 8所示, 随着结晶时间的增加, 合成产物的比表面积逐渐升高, 12 h下合成的NaY沸石的比表面积(630.25 m2·g-1)及孔容最大.另外, 6、8 h下合成的沸石具有相似的孔径分布, 微孔均分布在0.45~0.6 nm之间;10、12 h下合成的沸石具有相似的孔径分布, 微孔主要分布在0.6~0.9 nm, 但只有12 h下合成的沸石在1.2~1.8 nm间有微孔分布.因此, 水热结晶12 h下比较容易合成具有多级孔的NaY沸石.
| 表 6 不同晶化时间下合成的NaY沸石的比表面积及孔容分析 Table 6 Specific surface areas and pore volumes analysis of NaY zeolites synthesized by coal fly ash at different times |
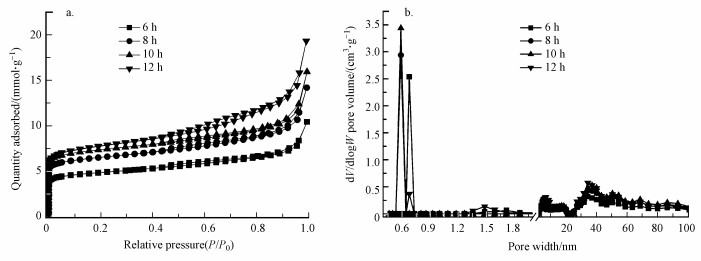 |
| 图 8 不同晶化时间下合成的NaY沸石的N2吸附/脱附等温线及孔径分布 Fig. 8 N2 adsorption/desorption isotherms and pore size distributions of NaY zeolites synthesized from coal fly ash at different times |
综上所述, 选用Si/Al比为2左右的粉煤灰, 在碱浓度为2 mol·L-1、温度为65 ℃的水热条件下结晶12 h, 是合成具有高比表面积NaY沸石的最佳合成条件.
3.5 NaY沸石吸附乙酸乙酯性能研究在不同水热温度下合成的粉煤灰源沸石相比于粉煤灰, 其比表面积和孔容均得到了很大的提升, 理论上比表面积更大的沸石对乙酸乙酯的吸附效果可能更佳.采用自制吸附评价装置对沸石进行吸附能力评价, 图 9为样品在125 ppm(相当于492 mg·m-3)浓度下的乙酸乙酯吸附穿透曲线.穿透时间定义为: 乙酸乙酯蒸气经过吸附剂吸附后, 出口气体浓度为进口气体浓度5%时的时间(即Ci/C0=0.05).穿透时间、吸附饱和时间和吸附容量的比较如表 7和图 9所示, 吸附饱和时间越长, 吸附性能越好.结果表明, CFAZ-Y65具有更好的吸附性能, 其中, CFAZ-1-Y65和CFAZ-2-Y65对乙酸乙酯的吸附容量最大, 分别为108.2 mg·g-1和106.6 mg·g-1, 分别是原粉煤灰的7倍和8倍.
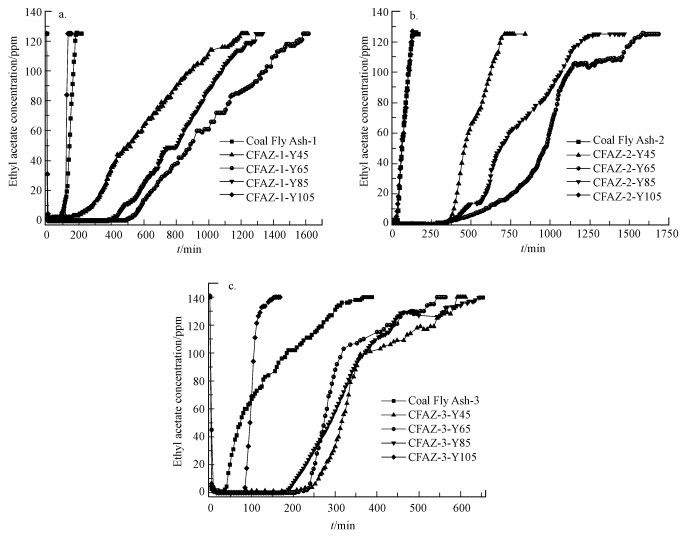 |
| 图 9 粉煤灰CFA-1/CFA-2/CFA-3及其不同水热温度下合成的沸石吸附乙酸乙酯动态吸附图 Fig. 9 Dynamic adsorption diagram of ethyl acetate adsorbed on coal fly ash CFA-1/CFA-2/CFA-3 and zeolites synthesized from CFA-1/CFA-2/CFA-3 at different hydrothermal temperatures |
| 表 7 CFA-1/CFA-2/CFA-3粉煤灰及其不同水热温度下合成的沸石的穿透时间、吸附饱和时间和吸附容量 Table 7 The breakthrough time, adsorption saturation time and adsorption capacity of from coal fly ash CFA-1/CFA-2/CFA-3 and zeolites synthesized at different hydrothermal temperatures from CFA-1/CFA-2/CFA-3 |
1) 硅铝比为1~2的粉煤灰均可在水热温度为65 ℃、碱浓度为2 mol·L-1的条件下结晶12 h后合成NaY沸石.硅铝比在1左右的粉煤灰合成的NaY沸石比表面积较小且有NaA沸石生成, 硅铝比在2左右的粉煤灰合成的NaY沸石的比表面积和孔容更大, 且对乙酸乙酯的吸附量更大.
2) 结晶温度对NaY沸石合成影响最大, 45 ℃下没有NaY沸石形成, 65 ℃下可成功合成NaY沸石, 85 ℃下有方钠石产生但大部分还是NaY沸石, 105 ℃下形成了低比表面积的方钠石.因此, 65 ℃是最有利于结晶过程中脱硅进而合成多级孔NaY沸石的温度.
3) 碱浓度对合成沸石影响很大, 低碱度下并没有合成NaY沸石且合成的产物比表面积太小, 不利于吸附乙酸乙酯;碱浓度过高则没有提高沸石的纯度且比表面积较小, 还浪费了材料, 因此, 2 mol·L-1是NaY沸石合成的最佳碱浓度.
4) 晶化时间对于合成NaY沸石有一定的影响, 晶化时间过短则不能合成高比表面积的NaY沸石, 晶化时间过长会导致能源的浪费.
Carlos A, Jenny A, AHM José, et al. 2012. A NaY zeolite synthesized from Colombian industrial coal by-products: Potential catalytic applications[J]. Catalysis Today, 190(1): 61-67. DOI:10.1016/j.cattod.2012.02.025 |
He D, Yuan D, Song Z, et al. 2016. Hydrothermal synthesis of high silica zeolite Y using tetraethylammonium hydroxide as a structure-directing agent[J]. Chemical Communications, 52(86): 12765-12768. DOI:10.1039/C6CC06786G |
Larsen S C. 2007. Nanocrystalline zeolites and zeolite structures: Synthesis, characterization, and applications[J]. The Journal of Physical Chemistry C, 111(50): 18464-18474. DOI:10.1021/jp074980m |
Li Q, Su G, Li C, et al. 2019. Emission profiles, ozone formation potential and health-risk assessment of volatile organic compounds in rubber footwear industries in China[J]. Journal of Hazardous Materials, 375: 52-60. DOI:10.1016/j.jhazmat.2019.04.064 |
刘思远, 郝瑞霞, 王丽沙, 等. 2019. 分子筛脱硅对其结构与吸附氨氮性能的影响[J]. 中国环境科学, 39(12): 5029-5039. |
Mu L, Feng W, Zhang H, et al. 2019. Synthesis and catalytic performance of a small crystal NaY zeolite with high SiO2/Al2O3 ratio[J]. Rsc Advances, 9(36): 20528-20535. DOI:10.1039/C9RA03324F |
Nigar H, Navascues N, de la Iglesia O, et al. 2015. Removal of VOCs at trace concentration levels from humid air by microwave swing adsorption, kinetics and proper sorbent selection[J]. Separation and Purification Technology, 151: 193-200. DOI:10.1016/j.seppur.2015.07.019 |
Padhy R R, Shaw R, Tiwari S, et al. 2015. Ultrafine nanocrystalline mesoporous NaY zeolites from fly ash and their suitability for eco-friendly corrosion protection[J]. Journal of Porous Materials, 22(6): 1483-1494. DOI:10.1007/s10934-015-0029-3 |
Qamar M, Baig I, Azad A M, et al. 2016. Synthesis of mesoporous zeolite Y nanocrystals in octahedral motifs mediated by amphiphilic organosilane surfactant[J]. Chemical Engineering Journal, 290: 282-289. DOI:10.1016/j.cej.2016.01.045 |
Ren X, Liu S, Qu R, et al. 2020. Synthesis and characterization of single-phase submicron zeolite Y from coal fly ash and its potential application for acetone adsorption[J]. Microporous and Mesoporous Materials, 295(1): 109940. |
Shen L, Xiang P, Liang S, et al. 2018. Sources profiles of volatile organic compounds (VOCs) measured in a typical industrial process in Wuhan, Central China[J]. Atmosphere, 9(8): 297. DOI:10.3390/atmos9080297 |
田亮, 魏巍, 程水源, 等. 2017. 典型有机溶剂使用行业VOCs成分谱及臭氧生成潜势[J]. 安全与环境学报, 17(1): 314-320. |
Wang H, Qiao Y, Chen C, et al. 2014. Source profiles and chemical reactivity of volatile organic compounds from solvent use in Shanghai, China[J]. Aerosol and Air Quality Research, 14(1): 301-310. DOI:10.4209/aaqr.2013.03.0064 |
谢轶嵩, 郑新梅, 刘春蕾. 2018. 南京市印刷行业VOCs成分谱及臭氧生成潜势[J]. 环境科技, 31(5): 68-71. |
翟增秀, 孟洁, 王亘, 等. 2018. 有机溶剂使用企业挥发性恶臭有机物排放特征及特征物质识别[J]. 环境科学, 39(8): 3557-3562. |
Zhang K, Fernandez S, Lawrence J A, et al. 2018. Organotemplate-free beta zeolites: From zeolite synthesis to hierarchical structure creation[J]. Acs Omega, 3(12): 18935-18942. DOI:10.1021/acsomega.8b02762 |
Zhang W, Qu Z, Li X, et al. 2012. Comparison of dynamic adsorption/desorption characteristics of toluene on different porous materials[J]. Journal of Environmental Sciences, 24(3): 520-528. DOI:10.1016/S1001-0742(11)60751-1 |
Zhao J, Yin Y, Li Y, et al. 2016. Synthesis and characterization of mesoporous zeolite Y by using block copolymers as templates[J]. Chemical Engineering Journal, 284: 405-411. DOI:10.1016/j.cej.2015.08.143 |
赵锐, 黄络萍, 张建强, 等. 2018. 成都市典型溶剂源使用行业VOCs排放成分特征[J]. 环境科学学报, 38(3): 1147-1154. |
赵书言. 2021. 煤炭行业: 碳中和背景下机遇与挑战并存, 供给收缩促龙头经营壁垒提升[R]. 中国银河: 发现报告
|
Zheng J, Yu Y, Mo Z, et al. 2013. Industrial sector-based volatile organic compound (VOC) source profiles measured in manufacturing facilities in the Pearl River Delta, China[J]. Science of the Total Environment, 456: 127-136. |
Zhou R, Zhang Q, Shao J, et al. 2012. Optimization of NaY zeolite membrane preparation for the separation of methanol/methyl methacrylate mixtures[J]. Desalination, 291: 41-47. DOI:10.1016/j.desal.2012.01.023 |
 2021, Vol. 41
2021, Vol. 41


