2. 安徽工业大学, 冶金减排与资源综合利用教育部重点实验室, 马鞍山 243002
2. Key Laboratory of Metallurgical Emission Reduction & Resources Recycling of Ministry of Education, Anhui University of Technology, Ma'anshan 243002
铅是一种可对人体健康造成严重危害的重金属元素.研究表明, 人体摄入铅主要滞留在骨骼中, 过量会严重损害大脑(梁奇峰等, 2003);当体内铅含量超过30%时, 则会造成婴幼儿生长迟缓、智力低下等严重后果.即使低浓度的铅也会通过长期累积对人体造成损害, 依据国家《污水排放综合标准》(GB8978—1996), 环境中铅的最高允许排放浓度为1 mg·L-1(李静文, 2013).因此, 开发对重金属Pb(Ⅱ)具有超高吸附容量的环境友好型吸附剂对人类生命健康和生态环境安全至关重要, 近年来已成为环境污染治理领域的研究热点.
在过去的几十年中, 科研人员先后开发出不同种类的吸附剂, 包括水凝胶(Kim et al., 2017)、粘土(Ding et al., 2014)、金属有机骨架(MOFs)(Chen et al., 2017)、碳基材料(Sun et al., 2019)和生物吸附剂(Hassan et al., 2020)等, 其中, 具有高比表面积、大孔体积且带有丰富功能团的吸附剂倍受青睐.但吸附剂的广泛应用受到不同条件的限制, 如吸附容量低、制备过程复杂或成本高昂等.与此相反, 矿物基吸附剂由于具有绿色环保、价格低廉且易于大规模生产等优点而广受推崇(Pasinszki et al., 2020).因此, 一些科研人员开始致力于开发这种资源储备丰富且处理效率极高的吸附剂.例如, 最新研制出的Fe-基和MnO2-基吸附剂对Pb2+表现出很好的吸附效果(Li et al., 2018);无定形碳酸钙材料也由于其较高的溶度积和出色的分散性被证实对重金属离子甚至放射性元素离子都具有超高的吸附能力(Lei et al., 2017; Cai et al., 2010).
磷酸钙类材料是生物医疗领域极其重要的生物材料(Jiao et al., 2016), 被广泛应用于组织工程(Yao et al., 2019)、药物运输(Wei et al., 2015)等方面.最近, 磷酸钙类材料(CaPs)也被用作吸附剂, 因其对重金属离子和有机污染物出色的吸附能力而被研究报道(Jiang et al., 2012; Li et al., 2015; Su et al., 2017).在众多磷酸钙材料中, 磷酸八钙(OCP)具有层状微结构, 包含相互交替的磷灰石层与水合层(Tseng et al., 2006).在临床医学领域, 因磷酸八钙具有优越的可吸收和骨诱导性, 常被用于骨修复治疗(Sugawara et al., 2013).相对而言, 有关磷酸八钙材料在污染物去除领域的研究报道较少(Zhang et al., 2015).相较于氧化石墨烯纳米片(Cao et al., 2019)、Ti3C2Tx(T=OH or F)(Ying et al., 2015)和层状双氢氧化物(Chen et al., 2015)等同样具有层状微结构的二维吸附剂材料, 推测磷酸八钙材料在环境污染物去除方面也具有很大的潜力.
基于此, 本研究采用仿生矿化的方法, 借助聚电解质PAH晶体生长调控剂, 合成中空、多孔磷酸八钙(OCP/PAH)超结构.同时, 对该矿物吸附剂的微观结构和空隙特性进行详细表征, 并将其用于处理含Pb(Ⅱ)的污染水体.以期为矿物吸附剂在水污染处理和环境保护等方面的应用提供参考.
2 材料和方法(Materials and methods) 2.1 实验原料与方法OCP/PAH样品采用气相扩散合成方法, 反应温度为(22±1) ℃(Su et al., 2016).具体操作为:将1 mg聚丙烯基铵盐酸盐(PAH, MW=15 kDa)加入到5 mL CaCl2溶液(40 mmol·L-1)中, 完全溶解后再加入5 mL NaH2PO4溶液(30 mmol·L-1), 搅拌均匀后转移至20 mL的小称量瓶中, 用封口膜完全封住称量瓶口, 用细针在封口膜上扎3个圆孔, 并放入气相反应器中.在气相反应前1 h, 反应器中提前放入含有20 mL氨水的称量瓶, 用封口膜封住瓶口, 并用针扎出均匀的圆孔.气相扩散6 h后, 样品在6000 r·min-1下离心分离, 所得样品用去离子水清洗3遍, 冷冻干燥过夜备用.
纯OCP样品借助微波水热合成.具体操作为:配置40 mmol·L-1的CaCl2溶液(5 mL), 再加入5 mL NaH2PO4溶液(30 mmol·L-1), 混合溶液在80 ℃微波水热条件下反应60 min;样品在6000 r·min-1下离心分离, 所得样品用去离子水清洗3遍, 冷冻干燥过夜备用.
2.2 Pb(Ⅱ)吸附实验以Pb(Ⅱ)为吸附实验的目标重金属污染物, 采用100 mL加塞锥形瓶进行间歇吸附实验.在每个装有100 mL不同浓度Pb(Ⅱ)溶液的锥形瓶中加入25 mg吸附剂, 200 r·min-1转速下, 避光在往复式空气浴振荡器中摇动.与吸附剂混合前, 用0.1 mol·L-1 HCl或0.1 mol·L-1 NaOH调节Pb(Ⅱ)溶液的pH值.Pb(Ⅱ)浓度采用ICP-OES进行测量.吸附完成后, 将所有的吸附残渣沉淀离心分离, 冷冻干燥一夜以备进一步表征.所有吸附实验均在25 ℃条件下进行, 且每组实验平行重复3次.
2.3 产物表征采用X射线衍射仪(Ultimate Ⅳ, 日本)对产物进行物相分析, 2θ为4°~80°, Cu靶, 仪器自带PDXL2相成分分析系统.采用JSM-6490LV型场发射扫描电镜(日本)对产物形貌和结构进行分析, 并用Jeol2010型透射电镜(日本)在200 kV下进行高分辨(HRTEM)和选区电子衍射(SAED)分析.借助红外光谱仪(Nicolet 6700, 美国)对样品中有机成分进行表征.采用Zetasizer Nano S90型动态光散射仪对样品的颗粒粒径及Zeta电位进行分析.采用赛默飞世尔科技公司的ESCALAB 250 Xi型X射线光电子能谱仪(XPS)对磷酸八钙样品的表面化学成分和化学形态进行表征.
3 结果与讨论(Results and discussion) 3.1 PAH调控下OCP吸附剂的合成仿生矿化合成的样品具有典型的微球结构, 直径为3~4 μm, 微球表面由相互交叉排列的纳米片组成多孔结构(图 1a).TEM图显示微球内部中空(图 1b), 包含一个直径约为1.5 μm的空腔;球壳厚度约为500 nm, 由长1 μm和厚20 nm超薄纳米片构筑而成.HRTEM图显示纳米片具有0.348和0.296 nm的晶格条纹, 分别对应于OCP的(020)和(060)晶面;有趣的是, 在纳米片边缘观察到较多的非晶纳米区域(图 1c), 直径约为5 nm.选取电子衍射花样也表明纳米片为典型的磷酸八钙单晶, 纳米片沿着c轴方向生长(图 1c插图).作为比较, 本研究采用微波水热合成的纯OCP样品具有不规则的花状结构(图 1d), 其组成单元为95 nm厚的纳米片(图 1e), 且其有向带状结构生长的趋势.
 |
| 图 1 不同方法合成的磷酸八钙(OCP)样品 (a, b.OCP/PAH花状结构的SEM和TEM图;c.超薄纳米片的高分辨透射电镜图, 嵌入图为相应的选区电子衍射花样;d, e.水热合成的纯OCP结构的SEM图和相应的放大图) Fig. 1 OCP/PAH samples prepared by different methods (a, b.SEM and TEM images of OCP/PAH; c.HRTEM image of a ultrathin nanosheet, the inset is the corresponding selected area electron diffraction (SAED) pattern; d, e. SEM and relevant magnified images of pure OCP synthesized by microwave hydrothermal method) |
本研究详细跟踪了OCP/PAH样品的生长过程.早期阶段, PAH与Na2HPO4溶液混合后, 由于PAH分子链含有—NH3+基团, 它会与磷酸根之间形成R-NH3+/H2PO4-复合物, 此时溶液逐渐变得乳浊.光学显微观察显示溶液形成了“囊泡”状结构(图 2a).动态光散射分析(DSL)表征该微结构在1.9 μm左右(图 2b).钙离子加入后, 颗粒尺寸变小至882 nm, 这主要由于Ca2+与PO43-在囊泡表面发生异相成核.偏光显微分析显示该颗粒未呈现双折射现象(插图 2c), 表明颗粒处于非晶状态, 应为无定形磷酸钙(马芳等, 2017).
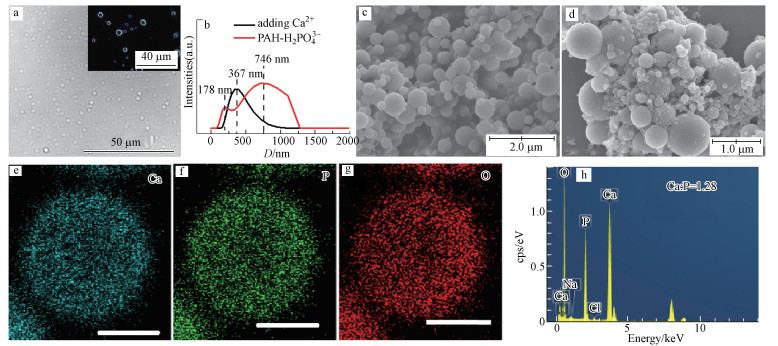 |
| 图 2 早期矿化溶液中形成矿化前驱物 (a.Ca2+/PAH/H2PO4-囊泡的光学图, 嵌入图为相应的偏光图;b.PAH/H2PO4-囊泡和加入钙离子后的粒径分布图;c, d.球状矿化前驱物在气相扩散前后的SEM图;e~h.前驱物的EDX元素分布图) Fig. 2 The self-assembled precursor in the early stage of mineralization (a.The optical image of Ca2+/PAH/H2PO4-, inset is the corresponding polarized image; b.The particle distribution of PAH/H2PO4- vesicles and samples after addition of Ca2+; c, d.SEM images of the spherical mineral precursor before the gas diffusion procedure(c), spherical samples after 1 h mineralization(d); e~h.EDX elemental mappings for the precursor) |
SEM图显示(图 2c)矿化溶液加入Ca2+后生成了直径约1 μm球状颗粒, 其表面光滑, 该结构对应于动态光散射跟踪到的直径为882 nm的颗粒.元素面扫描分析显示该结构内包含Ca、P和O等元素, EDX显示Ca/P约为1.28(图 2e~2h).FT-IR光谱显示(图 3d(I)), 由于存在HPO42-, PO4基团中P—O键非对称拉伸振动分裂为1044和951 cm-1处两个峰, 且O—P—O弯曲振动出现在564 cm-1处.上述分析均表明该产物为典型的无定形磷酸钙(Lu et al., 2019).而在气相扩散反应1 h后, 可观察到该微球表面逐渐变得粗糙(图 2d), 应为ACP逐渐向其它相转化.
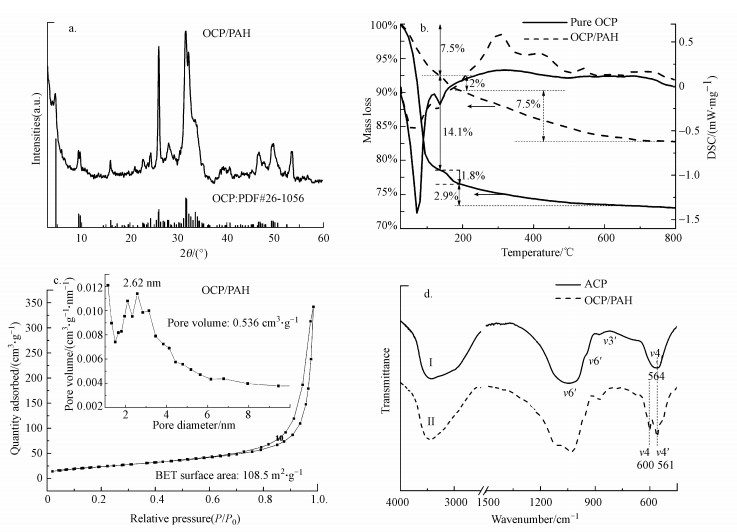 |
| 图 3 OCP/PAH样品不同表征的图谱 (a.XRD图;b. TG/DSC曲线;c.N2气吸附-脱附等温曲线和相应的孔径分布;d.早期前驱物和OCP/PAH的FT-IR光谱图) Fig. 3 Different spectra of OCP/PAH microspheres (a.the XRD pattern; b.TG/DSC curves; c.N2 adsorption-desorption isotherms curves and the corresponding pore diameter distribution; d.FT-IR spectra of OCP/PAH and early formed mineral precursor) |
气相扩散6 h后, 溶液中则可以观察到由纳米薄片构筑而成的多孔微球(图 1a~1b).XRD分析显示样品为典型的五水合磷酸八钙(Ca8H2(PO4)6·5H2O, JCPDS PDF#26-1056)(图 3a).红外谱图显示(图 3d(Ⅱ))典型的P—O弯曲振动峰在600 cm-1和561 cm-1处, 进一步证实了合成的样品为磷酸八钙.TG-DSC分析表明(图 3b), OCP/PAH失重分为3个阶段:第1个阶段发生在135 ℃之前, DSC显示为吸热反应, 失重是由于材料表面吸附水受热释放造成, 约占材料总质量的7.5%;第2次失重中心温度在178 ℃, 损失约为2%, 由磷酸八钙结构中HPO4—OH层的塌缩导致;最后阶段发生在200~700 ℃, 该阶段PAH发生热解, 且OCP转变为更稳定的HAP, 该阶段为典型的放热反应.在这一阶段高分子PAH分解引发了一个放热峰, 可推断PAH最大可占OCP/PAH超结构质量的4.3%, 虽然PAH的含量较低, 但其对OCP/PAH的形貌和孔结构调节都发挥着重要作用.
通过OCP/PAH微球的氮气吸附、解吸等温线(图 3c)可获得其比表面积和孔尺寸分布.在相对低压区域(P/P0 < 0.2), 样品的吸附状态呈缓增形式, 这是由于材料存在微孔.根据最新的IUPAC分类, 该等温线可归类为Ⅱ类(Thommes et al., 2015).等温线在相对高压区域(P/P0=0.4~1.0)时, 展现出典型的H4型迟滞回线, 这与纳米片组装的空心腔和介孔壁有关.孔径分析(图 3c中插图)显示OCP/PAH包含丰富的介孔(2.0~4.1 nm), 孔径集中在2.62 nm, 其BET比表面积达到108.5 m2·g-1.该结构具有较高的比表面积和丰富的介孔结构, 非常利于离子的吸附、扩散和交换.
4 OCP/PAH超结构对Pb(Ⅱ)的吸附(The adsorption of OCP/PAH superstructures towards Pb(Ⅱ)) 4.1 不同因素对Pb(Ⅱ)吸附的影响在较低的pH值(< 4.0)条件下, 重金属离子与溶液中的质子间存在竞争性吸附, 导致吸附剂去除效率显著降低(图 4a).同时, 低pH值易导致OCP/PAH结构的酸解.另一方面, 高pH值(>6.0)也可能不利于吸附, 此时重金属会形成不溶性氢氧化物(Sitko et al., 2013).实验显示当pH值保持在4.0~8.0时, 吸附剂对Pb(Ⅱ)保持着较高的吸附容量.为了避免可能的干扰, 吸附实验中最佳pH值范围选择为4.0~6.0.除特别说明外, 所有吸附实验均在pH=5.5下开展.
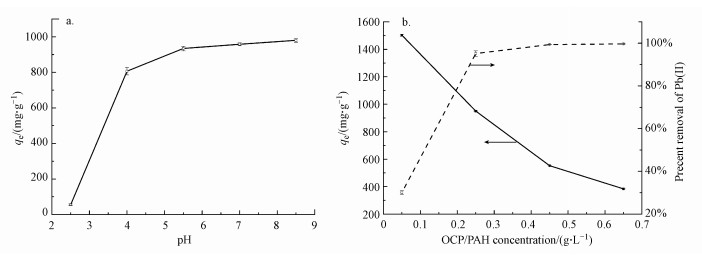 |
| 图 4 不同初始条件对吸附容量的影响 (a.pH;b.OCP/PAH浓度) Fig. 4 The effect of different initial condition on the adsorption capacity |
本研究进一步评估了不同剂量的OCP/PAH对重金属Pb(Ⅱ)吸附的影响(图 4b).当OCP/PAH为0.05 g·L-1时, 吸附剂用量明显不足.当吸附剂用量增加到高于0.25 g·L-1时, 吸附能力显著提高, 吸附剂对重金属的去除率可达95%以上.虽然较大的吸附剂用量有利于对污染物的高效去除, 但这也会显著降低吸附剂的利用率.因此, 本研究选择0.25 g·L-1作为最佳吸附剂初始浓度.
4.2 吸附等温线通常情况下, 吸附等温线可在很大程度上反映平衡状态下吸附剂与金属离子间的相互作用特征, 并可估算出最大吸附容量.典型的吸附等温曲线如图 5a所示, 分别采用Langmuir和Freundlich模型分析了污染物的吸附等温线(图 5b和5c).OCP/PAH对Pb(Ⅱ)的吸附更符合Langmuir吸附模式, 即吸附过程为典型的单分子层吸附.根据Langmuir模型的拟合结果, Pb(Ⅱ)的最大吸附量(qmax)为1644.74 mg·g-1(表 1).
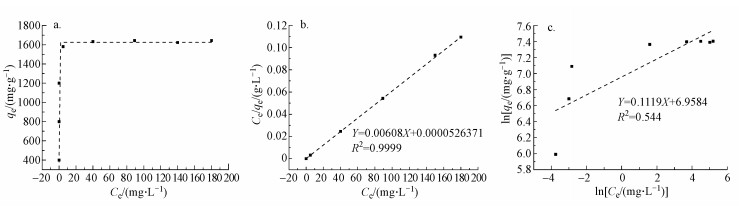 |
| 图 5 等温吸附曲线 (a.OCP/PAH吸附Pb(Ⅱ)的吸附等温曲线, b.Langmuir模型拟合曲线, c.Freundlich模型拟合曲线) Fig. 5 Adsorption isotherms curve (a.Adsorption isotherms curve of Pb(Ⅱ) onto OCP/PAH; b.The fitting curves by Langmuir model, c.The fitting curves by Freundlich model) |
| 表 1 采用Langmuir和Freundlich模型拟合的吸附平衡参数 Table 1 The fitting parameters of adsorption equilibrium using Langmuir and Freundlich models |
本研究进一步研究了OCP/PAH对Pb(Ⅱ)吸附过程的动力学特征(图 6a), 并采用准一级和准二级吸附动力学方程对数据进行了拟合(图 6b).相应的动力学拟合参数在表 2中列出, 结果显示, 吸附动力学数据很好地符合准二级动力学方程, R2达到0.99988.
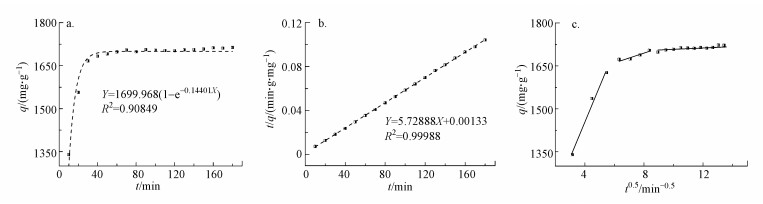 |
| 图 6 OCP/PAH吸附动力学曲线 (a.准一级动力学模型;b.准二级动力学模型;c.颗粒内扩散模型;[Pb2+]=500 mg·L-1) Fig. 6 Adsorption kinetics fitting curves of OCP/PAH (a.pseudo-first-order; b.pseudo-second-order; c.intra-particle diffusion equations) |
| 表 2 采用准一级、准二级动力学方程拟合的吸附动力学参数 Table 2 The fitting parameters of adsorption kinetics using the pseudo-first-order, pseudo-second-order equations |
进一步借助颗粒内扩散模式分析吸附动力学数据, 以确定其控制步骤(图 6c).从图中可以看出, 曲线并未经过坐标原点, 且存在多个线性区域, 说明吸附速率不是由颗粒内扩散过程控制的, 而是一个多步骤的吸附过程.整个吸附过程可分为3个阶段:第1阶段为快速吸附过程, 得益于吸附质的快速扩散和丰富的外表面吸附位点;第2阶段吸附质缓慢扩散到孔隙中, 并被内表面吸附, 这是由于OCP/PAH几乎所有的外表面都被吸附质覆盖;最后阶段为离子交换或络合过程, 需要更长的时间达到平衡.
5 OCP/PAH的吸附机理(The adsorption mechanism of OCP/PAH)借助不同的表征手段进一步探究Pb2+与吸附剂之间的吸附机理.Zeta电位分析显示(图 7), 在pH=2.5~8.5条件下, OCP/PAH样品表面呈正电荷, 且均在+10 eV以上;而微波水热合成的纯OCP样品的电位接近零.显然, 表面带正电荷的OCP/PAH与Pb2+存在库伦斥力, OCP/PAH对Pb2+优越的吸附特性应与样品的表面电荷无关.
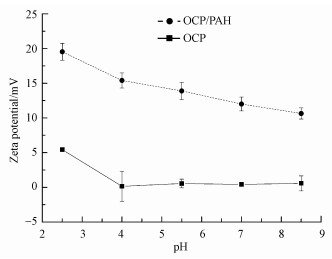 |
| 图 7 不同pH值下OCP/PAH的Zeta电位 (COCP/PSS=1 g·L-1) Fig. 7 Zeta potential of OCP/PAH under different pH values (COCP/PSS=1 g·L-1) |
借助XPS进一步对吸附前后样品的表面化学进行了表征.吸附后的样品中可明显检测到Pb 4f的峰值(图 8a~8b), 表明重金属离子Pb2+被样品吸附.且吸附后Ca 2p峰的相对强度降低(图 8c), 相应的峰被转移到更高的结合能, 表明Ca2+与金属离子之间发生了离子交换(Liu et al., 2019).通过计算可以分别得出Ca 2p1/2和Ca 2p3/2吸附Pb(Ⅱ)后前后的结合能差, 该结合能差仅分别为0.11 eV和0.1 eV.前期研究中发现, OCP样品对Cu(Ⅱ)和Cd(Ⅱ)吸附前后的结合能差异分别为0.37和0.18 eV(Zhu et al., 2020);相比较而言, 吸附Pb(Ⅱ)后结合能变化非常小, 表明Pb(Ⅱ)取代Ca(Ⅱ)后金属离子所处的化学环境变化较小.
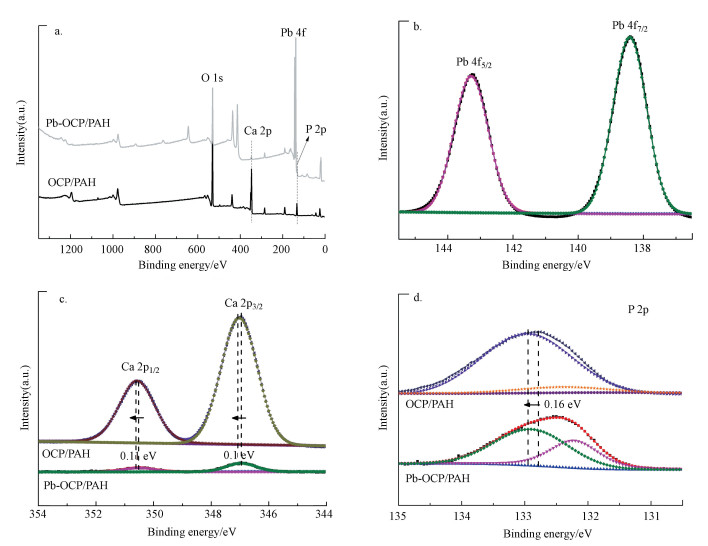 |
| 图 8 OCP/PAH吸附前后的XPS谱图 (a.OCP/PAH样品吸附前后的高分辨XPS图;b.Pb 4f;c.Ca 2p;d. OCP/PAH样品吸附Pb2+前后的P 2p图) Fig. 8 High-resolution XPS spectra of OCP/PAH samples (a.XPS image before and after the adsorption, b.Pb 4f, c.Ca 2p, d.P 2p for OCP/PAH before and after the adsorption of Pb2+) |
同时, 高分辨XPS谱图中P 2p在Pb(Ⅱ)吸附后分解为两个峰, 分别对应于OCP中的PO4和含Pb的磷酸盐相.吸附后P 2p峰的强度降低, 表明OCP中的P因离子交换而转移到更高的结合能处(图 8c);XRD图(图 9)证实此时形成了新的物相Ca2.5Pb7.5(OH)2(PO4)6.综上分析, 可推断OCP/PAH对Pb2+的吸附机理为材料表面的Ca2+与Pb2+发生了离子交换, 由于吸附前后活性中心PO4周围的化学环境变化较小, 利用该交换过程的发生, 从而使得吸附容量变得非常大.
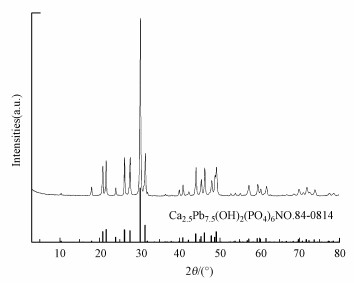 |
| 图 9 OCP/PAH吸附Pb(Ⅱ)后的XRD图谱 Fig. 9 XRD patterns of OCP/PAH after adsorption of Pb(Ⅱ) |
将OCP/PAH样品与前期合成的多孔的羟基磷灰石(HAP)吸附剂进行比较(Su et al., 2019), 后者的最大吸附容量仅为210 mg·g-1, 这表明亚稳相的OCP比晶体HAP作为吸附剂更具有优势.进一步将其与微波水热合成的OCP进行比较, 后者的最大吸附容量为1081 mg·g-1, 显然也低于OCP/PAH样品.这种差异应源于其结构差异, 水热合成的OCP纳米片较厚, 这在一定程度上限制了Pb(Ⅱ)的扩散和交换;而仿生矿化合成的纳米片超薄, 且结构内有一定的非晶区域, 这显然利于Pb(Ⅱ)与Ca(Ⅱ)之间的交换.同时, 仿生合成样品的多孔、中空特性也应对吸附有贡献.
6 结论(Conclusions)1) 借助仿生矿化手段, 在PAH调控下可以较容易地制备由超薄纳米片构筑的中空、多孔OCP/PAH吸附剂.实验结果显示, PAH/PO43-囊泡结构为早期无定形磷酸钙异相成核提供模板, 球状无定形磷酸钙前驱物经历熟化过程并最终生长为中空、多孔超OCP结构.
2) OCP/PAH吸附剂具有较高的比表面积和丰富的孔径结构, 是优良的矿物吸附剂;其对重金属离子Pb2+具有优越的吸附活性, qmax可以达到1644.74 mg·g-1.吸附动力学过程符合准二级动力学模式, 吸附等温曲线符合Langmuir模式, 即重金属吸附属于单分子层化学吸附, 吸附过程主要为金属离子与磷酸八钙表面的Ca2+进行离子交换.
3) OCP/PAH对Pb(Ⅱ)的高吸附容量得益于离子交换前后离子所处的化学环境变化较小, 并与中空、多孔、超薄纳米片和非晶微区密切相关.该吸附剂合成简单、易于批量化合成且吸附能力优越, 在污染物去除领域具有广阔的应用前景.
Cai G B, Zhao G X, Wang X K, et al. 2010. Synthesis of polyacrylic acid stabilized amorphous calcium carbonate nanoparticles and their application for removal of toxic heavy metal ions in wate[J]. The Journal of Physical Chemistry C, 114: 12948-12954. |
Cao M L, Li Y, Hong Y, et al. 2019. Functionalized graphene nanosheets as absorbent for copper(Ⅱ) removal from water[J]. Ecotoxicology and Environmental Safety, 173: 28-36. DOI:10.1016/j.ecoenv.2019.02.011 |
Ding D H, Lei Z F, Yang Y N, et al. 2014. Efficiency of transition metal modified akadama clay on cesium removal from aqueous solutions[J]. Chemical Engineering Journal, 236: 17-28. DOI:10.1016/j.cej.2013.09.075 |
Hassan M, Naidu R, Du J H, et al. 2020. Critical review of magnetic biosorbents: Their preparation, application, and regeneration for wastewater treatment[J]. Science of the Total Environment, 702: 134893. DOI:10.1016/j.scitotenv.2019.134893 |
Jiang, S D, Yao Q Z, Zhou G T, et al. 2012. Fabrication of hydroxyapatite hierarchical hollow microspheres and potential application in water treatment[J]. The Journal of Physical Chemistry C, 116: 4484-4492. |
Jiao K, Niu L N, Ma C F, et al. 2016. Complementarity and uncertainty in intrafibrillar mineralization of collagen[J]. Advanced Functional Materials, 26: 6858-6875. DOI:10.1002/adfm.201602207 |
Kim Y H, Kim Y K, Kim S J, et al. 2017. Nanostructured potassium copper hexacyanoferrate-cellulose hydrogel for selective and rapid cesium adsorption[J]. Chemical Engineering Journal, 313: 1042-1050. DOI:10.1016/j.cej.2016.10.136 |
Lei Z Y, Sun S T, Wu P Y. 2017. Ultrafast, Scale-up synthesis of pure and stable amorphous carbonate mineral nanoparticles[J]. ACS Sustainable Chemistry & Engineering, 5: 4499-4504. |
Li C F, Ge X L, Li Y D, et al. 2015. Modulation of release behaviors of methylene blue from degradable silica-methylene blue@octacalcium phosphate powders with different shell structures[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 472: 78-84. DOI:10.1016/j.colsurfa.2015.02.041 |
李静文. 2013. 硫化钠沉淀法处理含铅废水研究[J]. 赤峰学院学报(自然科学版), 29(1): 8-10. |
Li Y Z, Zhao R, Chao S, et al. 2018. Polydopamine coating assisted synthesis of MnO2 loaded inorganic/organic composite electrospun fiber adsorbent for efficient removal of Pb2+ from water[J]. Chemical Engineering Journal, 344: 277-289. DOI:10.1016/j.cej.2018.03.044 |
梁奇峰, 李京雄, 丘基祥. 2003. 环境铅污染与人体健康[J]. 广东微量元素科学, (7): 57-60. DOI:10.3969/j.issn.1006-446X.2003.07.012 |
Liu X M, Song K N, Liu WZ, et al. 2019. Removal and recovery of Pb from wastewater through a reversible phase transformation process between nano-flower-like Mg(OH)2 and soluble Mg(HCO3)2[J]. Environmental Science: Nano, 6: 467-477. DOI:10.1039/C8EN01173G |
Lu B Q, Garcia N A., Chevrier D M., et al. 2019. Short-range structure of amorphous calcium hydrogen phosphate[J]. Crystal Growth & Design, 19: 3030-3038. |
马芳, 崔名芳, 朱建华, 等. 2017. 聚烯丙基氯化铵调控下多孔羟基磷灰石微球的合成及作为药物载体的应用研究[J]. 无机材料学报, 32(11): 1215-1222. |
Pasinszki T, Krebsz M, Chand D, et al. 2020. Carbon microspheres decorated with iron sulfide nanoparticles for mercury(Ⅱ) removal from water[J]. Journal of Materials Science, 55: 1425-1435. DOI:10.1007/s10853-019-04032-3 |
Sitko R, Turek E, Zawisza B, et al. 2013. Adsorption of divalent metal ions from aqueous solutions using graphene oxide[J]. Dalton Transactions, 42: 5682-5689. DOI:10.1039/c3dt33097d |
Su Y P, Cui M F, Zhu J H, et al. 2016. Self-organized spatial patterns of carbonate formed via a nonclassical crystallization pathway[J]. Cryst Eng Comm, 18: 8726-8730. DOI:10.1039/C6CE01744D |
Su Y P, Cui M F, Zhu J H, et al. 2017. A facile synthesis of nanosheet-structured barium carbonate spheres with a superior adsorption capacity for Cr(Ⅵ) removal[J]. Journal of Materials Science, 53: 4078-4088. DOI:10.1007/s10853-017-1861-4 |
Su Y P, Wang J, Li S, et al. 2019. Self-templated microwave-assisted hydrothermal synthesis of two-dimensional holey hydroxyapatite nanosheets for efficient heavy metal removal[J]. Environmental Science Pollution Research International, 26: 30076-30086. DOI:10.1007/s11356-019-06160-4 |
Sugawara A, Asaoka K, Ding S J. 2013. Calcium phosphate-based cements: Clinical needs and recent progress[J]. Journal of Materials Chemistry B, 1: 1081-1089. DOI:10.1039/C2TB00061J |
Sun Y B, Wu Z Y, Wang X X, et al. 2019. Correction to macroscopic and microscopic investigation of U(Ⅵ) and Eu(Ⅲ) adsorption on carbonaceous nanofibers[J]. Environmental Science & Technology, 53: 11613. |
Thommes M, Kaneko K, Neimark A V, et al. 2015. Physisorption of gases, with special reference to the evaluation of surface area and pore size distribution (IUPAC Technical Report)[J]. Pure and Applied Chemistry, 87: 1051-1069. DOI:10.1515/pac-2014-1117 |
Tseng Y H, Mou C Y, Chan J C C. 2006. Solid-State NMR study of the transformation of octacalcium phosphate to hydroxyapatite: a mechanistic model for central dark line formation[J]. Journal of the American Chemical Society, 128: 6909-6918. DOI:10.1021/ja060336u |
Wei J, Shi J, Wu Q, et al. 2015. Hollow hydroxyapatite/polyelectrolyte hybrid microparticles with controllable size, wall thickness and drug delivery properties[J]. Journal of Materials Chemistry B, 3: 8162-8169. DOI:10.1039/C5TB01268F |
Yao S, Lin X F, Xu Y F, et al. 2019. Osteoporotic bone recovery by a highly bone-inductive calcium phosphate polymer-induced liquid-precursor[J]. Advanced Science, 6: 1900683. DOI:10.1002/advs.201900683 |
Ying Y L, Liu Y, Wang X Y, et al. 2015. Two-dimensional titanium carbide for efficiently reductive removal of highly toxic chromium(Ⅵ) from water[J]. ACS Applied Materials & Interfaces, 7: 1795-1803. DOI:10.1021/am5074722 |
Yu C F Chen F, Zhang S H, et al. 2017. Facile fabrication of multifunctional metal-organic framework hollow tubes to trap pollutants[J]. Journal of the American Chemical Society, 139: 16482-16485. DOI:10.1021/jacs.7b10265 |
Yu C, Tan C L, Zhang H, et al. 2015. Two-dimensional graphene analogues for biomedical applications[J]. Chemical Society Reviews, 44: 2681-2701. DOI:10.1039/C4CS00300D |
Zhang G, Delgado-López J M, Duane C L, et al. 2015. Growth behavior of monohydrocalcite (CaCO3·H2O) in silica-rich alkaline solution[J]. Crystal Growth & Design, 15: 564-572. |
Zhu J H, Shu J C, Yue X J, et al. 2020. Hollow and porous octacalcium phosphate superstructures mediated by the polyelectrolyte PSS: a superior removal capacity for heavy metal and antibiotics[J]. Journal of Materials Science, 55: 7502-7517. DOI:10.1007/s10853-020-04539-0 |
 2021, Vol. 41
2021, Vol. 41


