微塑料(Microplastics, MPs)是一类颗粒直径小于5 mm的塑料颗粒的统称, 最早被发现存在于海洋环境中(Thompson et al., 2004).MPs主要来源于塑料制品的破碎和降解, 以及日常护理产品如面部磨砂膏、牙膏等中的携带细小塑料颗粒等(Cole et al., 2011;Godoy et al., 2019;周泽妍等, 2021).最新研究发现, 微塑料同样普遍存在于河流、湖泊和河口等淡水环境中(Browne et al., 2011;Wagner et al., 2014).据报道, 珠江地表水中的MPs丰度约为379~7924个·m-3, 其中MPs的主要类型是聚丙烯(Polypropylene, PP)和聚乙烯(Polyethylene, PE)(Lin et al., 2018).由于塑料产品的使用量增加, 进入淡水环境的MPs数量不断增加(Connors et al., 2017), 可能对淡水生态系统产生较大的影响(Canniff et al., 2018;Wu et al., 2019;张子琪等, 2020).
微塑料由于其不规则的表面结构和较大的比表面积, 可以作为重金属污染物的载体, 影响它们在环境中的迁移行为(Holmes et al., 2012;Wang et al., 2020;李文华等, 2020;薛向东等, 2020).微塑料吸附行为主要受到吸附剂和吸附质本身的特性影响, 如微塑料容易在光照作用下发生老化(Yang et al., 2019),
导致其比表面积的增加和含氧官能团的形成, 从而增强了吸附能力(Holmes et al., 2014).Deng等(2017)研究表明, 老化后的低密度聚乙烯(Low Density Polyethylene, LDPE)对金属(Cu2+、Pb2+、Zn2+、Mg2+)的吸附能力是原始LDPE的5倍.Brennecke等(2016)发现, 老化聚氯乙烯(Polyvinyl chloride, PVC)由于比表面积增加和分子极性改变, 使得对Cu2+的吸附能力比原始聚苯乙烯(Polystyrene, PS)更大.因此研究光照老化作用对微塑料表面形貌、主要官能基团组成、表面电荷、极性等的变化影响, 并进一步阐明光照后微塑料对其他污染物吸附作用机制, 可以为深入研究实际环境中的微塑料对其他污染物的环境影响行为提供理论依据.同时, 多元复合污染体系对微塑料吸附过程也会产生较大影响, Huang等(2019)研究表明, 在铁离子存在下, LDPE表面吸附的金属(Cu2+、Pb2+、Mn2+、Zn2+)的总质量从653.67 μg·m-2减少至602.21 μg·m-2.环境中的重金属种类众多, 且往往以多种重金属共存体系为主, 而由于多组分重金属离子对吸附位点的竞争吸附作用, 会影响微塑料对重金属的吸附能力, 因此研究受光照老化影响后的微塑料对复合体系中重金属的吸附行为和竞争机制, 可以为多组分重金属体系中微塑料存在的影响作用提供理论参考.
微塑料由于其对其他污染物如重金属的吸附性能, 在水体中容易对生态效应产生较大影响作用(Hodson et al., 2017;Prata et al., 2019).Zhu等(2019)研究表明, 由于MPs对抗菌剂三氯生的高吸附能力, 使得MPs和三氯生对微藻的联合毒性相比单一的三氯生有明显降低.Bellingeri等(2019)则发现, 单独的纳米PS与纳米PS与重金属Cu2+联合作用相比, 对藻类生长没有明显的区别.然而, MPs与其他污染物对藻类的联合作用研究较少(Prata et al., 2019), 因此, 需要研究微塑料与其他污染物复合体系对生态系统的毒性效应具有重要的研究意义.
本文选择了被广泛应用于食品包装、容器、农用薄膜等的PP和PE材料作为吸附剂(Panti et al, 2019), 研究微塑料对两种典型的重金属离子Cu2+和Zn2+ (Calderon et al., 2015)的竞争吸附过程, 主要研究内容包括:①对比研究两种紫外光老化后的PE和PP微塑料对单一和二元复合体系中的Cu2+和Zn2+的吸附性能;②通过研究吸附动力学和吸附热力学行为及表面分析等手段, 分析MPs对重金属的吸附机制;③研究了MPs负载Cu2+或/和Zn2+金属离子对淡水藻类莱茵衣藻(C. reinhardtii)生长抑制作用和酶活性的影响.本文为深入研究MPs存在下对其他污染物的环境行为影响, 及探究微塑料与其他污染物共存体系下的联合生态效应提供理论依据.
2 材料和方法(Materials and methods) 2.1 试验材料Cu(NO3)2·3H2O和Zn(NO3)2·6H2O试剂均采购于国药集团, 称取一定量的试剂分别配制Cu2+和Zn2+浓度为500 mg·L-1的母液, 并用超纯水进行稀释成为一定浓度的标准使用液.
将颗粒大小约为10~20 μm的PE和PP微塑料粉末(广东东莞兴旺塑料制品有限公司)用95%乙醇洗涤, 然后用2%的HNO3溶液洗涤, 以去除微塑料中的有机杂质和金属离子.最后, 用超纯水洗涤3次后自然干燥.在实验室条件下, 使用UVB-313紫外灯对MPs进行均匀老化, 以模拟MPs在自然界中光照老化过程, 老化时间为600 h(Huang et al., 2019), 在吸附试验中均使用老化后的MPs材料.
2.2 微塑料的表征与分析利用Brunauer-Emmett-Teller(BET)(ASAP 2460, Micromeritics, USA)测定微塑料的比表面积和孔分布特性, 采用扫描电镜(SEM)(JMS-6490LV, JEOL, 日本)和傅里叶变换红外光谱仪(FT-IR)(Nicolet6700, ThermoScientific, 美国)对微塑料的微观形貌和主要官能团的变化进行了分析.
2.3 微塑料吸附重金属离子试验 2.3.1 吸附动力学试验在单一体系和二元复合体系中, Cu2+和Zn2+的初始浓度均为5 mg·L-1, 其中在二元体系里, m(Cu2+)∶m(Zn2+)=1∶1.MPs的投加量均为10 g·L-1, 重金属溶液的初始pH值调整至6.0, 将锥形瓶放置在恒温摇床中振荡, 振荡速度为150 r·min-1, 摇床温度恒定为298 K, 分别在不同吸附时间对微塑料进行取样, 称取一定质量(m)干燥后的微塑料样品, 放置到PTFE管中, 加入10 mL 20%浓度的王水溶液, 在室温条件下振荡24 h后, 在120 W的功率条件下超声处理1 h, 然后对样品进行过膜(0.22 μm醋酸纤维膜)处理, 脱附液经稀释后使用电感耦合等离子体发射光谱(ICP-OES, Thermo, 美国)分析金属离子浓度.
2.3.2 吸附等温线试验准确配置不同浓度梯度的单一金属离子和二元复合离子溶液, 其中在二元体系中, Cu2+和Zn2+的质量比保持为1∶1, 在相同投加量(10 g·L-1)的条件下, 测定PP和PE对金属离子的平衡吸附量Q(μg·g-1), 其计算公式见式(1).
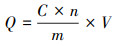
|
(1) |
式中, C为测定溶液中金属离子的浓度(μg·g-1);n为稀释倍数;V为脱附液的体积(L);m为吸附剂的质量(g).
2.3.3 吸附热力学试验在吸附热力学试验中, 准确配置不同浓度梯度的单一金属离子和二元复合离子溶液, 试验温度分别为288、298和308 K, 分别测定不同温度条件下和不同离子浓度下, PP和PE对两种金属离子Cu2+和Zn2+的平衡吸附量Q(μg·g-1).
2.3.4 pH值对微塑料吸附能力的影响采用2%的HNO3和2%的NaOH溶液来调节水溶液中pH值为3~6, 当MPs的投加量为10 g·L-1时测定在不同pH值条件下, PP和PE对重金属离子Cu2+和Zn2+在单一体系和二元体系的平衡吸附量, 其中单一和复合体系中Cu2+和Zn2+的浓度均为5 mg·L-1, 振荡一定时间达吸附平衡后, 测定溶液中的重金属离子浓度.
2.4 MPs与藻类的相互作用以莱茵衣藻(C. reinhardtii)为典型模型生物, 研究了MPs吸附金属离子后对水生生物的毒性作用.莱茵衣藻购买自武汉水生生物研究所.藻种培养在250 mL的锥形烧瓶中加入100 mL WC*培养基(Ma et al., 2016), pH值为7.0.在毒性实验中, 为了避免金属离子的干扰, 将硫酸铜和硫酸锌以及EDTA二钠从培养基中去除.藻类生长在室温下的振荡培养箱中, 光照强度为50 μmol·m-2·s-1, 光照时间为12 h/12 h的光/暗循环, 转速为150 r·min-1.烧瓶被随机放置在培养箱中.莱茵衣藻的初始细胞密度为2×105 cells·mL-1.
将吸附重金属离子达吸附平衡后的老化PP和PE微塑料(吸附试验过程参见2.3节)经过过滤和干燥后, 分别命名为PP-Cu、PP-Zn、PP-Cu-Zn、PE-Cu、PE-Zn和PE-Cu-Zn, 分别将不同的材料加入到藻液中, 并与吸附前的MPs进行了对比研究.在毒性实验中微塑料的浓度均为5 mg·L-1.在振荡培养箱中培养24、48、72和96 h后, 用Leica DM3000倒置显微镜(Leica Microsystems, Frankfurt, Germany)和颗粒计数仪分别计算藻类在微塑料胁迫下的细胞密度变化.藻类的生长抑制率(IR)由式(2)计算.
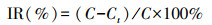
|
(2) |
式中, C为对照组的细胞密度(cells·mL-1), Ct分别为不同处理时间下的细胞密度(cells·mL-1).
2.5 酶活性测定藻的酶活性包括SOD、MDA和CAT的检测试剂盒购自南京建成生物工程研究所(中国南京).将5 mL藻液离心, 用磷酸盐缓冲液(PBS)洗涤.粉碎、离心后制备的藻液上清液置于冰箱中, 避光保存.分别加入试剂后, 用酶标仪(Synergy H1, BioTek, USA)分别在450、532和405 nm处测定SOD、MDA和CAT.
2.6 统计分析本实验都使用3次实验后取平均值, 表示为Mean±SD表示.图形绘制使用Origin9.0软件. 采用SPSS 22.0软件对毒性试验数据结果进行统计学分析, 当p值< 0.05时, 不同处理组间具有显著性差异性.
3 结果与讨论(Results and discussion) 3.1 老化后PP和PE微塑料的表征分析结果经过比表面积分析仪分析结果得到, 老化后PP和PE的比表面积分别为4.31 m2·g-1和3.39 m2·g-1, 均大于未老化前的MPs(表 1).该结果证明了光照老化会增加微塑料的表面粗糙度并显著提高其比表面积.利用老化前后PP和PE的FT-IR红外光谱图(图 1)对比研究, 结果发现, 经过老化后的PP和PE分别在1713 cm-1和1710cm-1处发现明显的CO伸缩振动峰, 表明在老化过程中发生了氧化反应, 在微塑料表面引入了羰基官能团.同时, 老化后的PE在1036cm-1处产生了明显的饱和—CH3吸收峰, 说明PE老化后饱和—CH3的含量增加.在1713 cm-1位置处有明显的吸收峰的出现, 文献资料表明, 此处吸收峰的产生是因为材料中出现了CO基团, 而在Virgin-PE材料中, 无对应官能团的出现, 说明UV老化作用确实在PE微塑料的表面产生了羰基, 证明了紫外光照的老化效果;老化后的PP与未老化的PP相比, 在1736 cm-1和1168 cm-1位置处的吸收峰明显增强, 即老化后的C—O官能团增加, 进一步证明了老化对PP的影响.此外, 采用羰基指数(Carbonyl Indices, Ico)对比了两种微塑料的老化程度(Prata, 2019), 通过式(3)得到, 老化后PP和PE的Ico指数分别为0.474和0.291, 即相同紫外老化条件下, PP的老化程度大于PE, 这可能由于PE的主链中含有仲碳, 相比PP中的叔碳不容易被氧化, 因此PE稳定性高于PP(Gewert et al., 2015).

|
(3) |
| 表 1 微塑料的孔隙结构参数 Table 1 Pore structure parameters of microplastics |
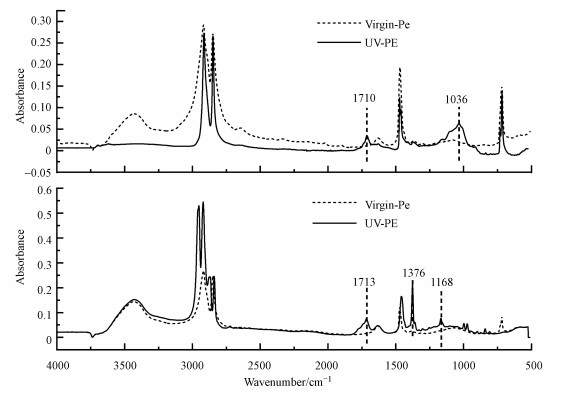 |
| 图 1 紫外光老化前后微塑料的红外光谱图 Fig. 1 FT-IR of microplastics before and after U-aging |
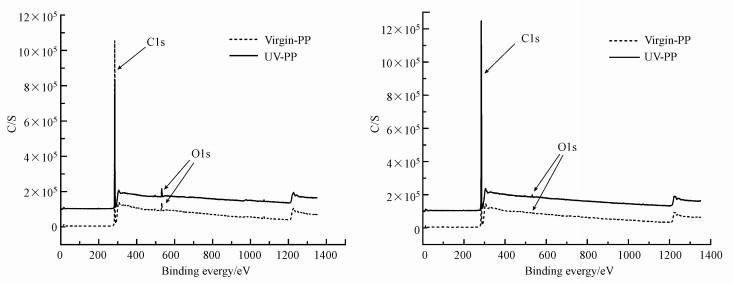 |
| 图 2 不同微塑料老化前后的XPS全谱分析图 Fig. 2 XPS spectra before and after U-aging of different MPs |
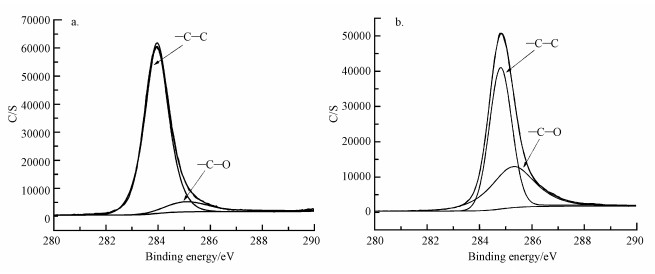 |
| 图 3 微塑料PP的C1s谱图分析 (a.老化前, b.老化后) Fig. 3 Peak value of C1s before(a) and after(b) U-aging by PP |
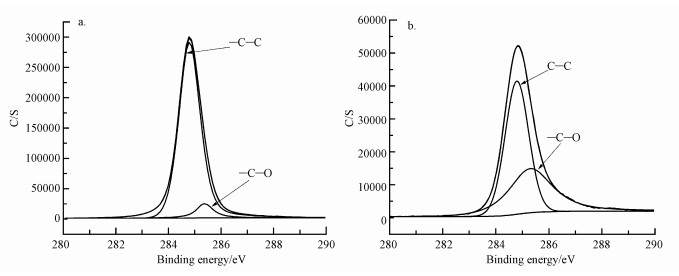 |
| 图 4 微塑料PE的C1s谱图分析 (a.老化前, b.老化后) Fig. 4 Peak value of C1s before(a) and after(b) U-aging by PE |
式中, ①为羰基峰的吸光度值;②为不同的材料参考峰处的吸光度值.
通过老化前后XPS谱图分析, 进一步发现, 老化前后材料表面的元素组成主要为C和O(结合能分别为284 eV和531 eV), 老化前O元素可能来源于材料制备过程中添加剂的加入(Dong et al., 2019);老化后的氧元素主要来源于微塑料表面含氧官能团, 如C=O, C—O等, 且老化后含氧基团的峰相对强度明显变强, 进一步验证了光氧化作用使得微塑料表面引入了含氧基团.
3.2 吸附动力学通过研究老化前后不同微塑料在单一和二元体系中对Cu2+和Zn2+的吸附动力学过程(图 5), 并利用拟一级吸附动力学方程(式(4))和拟二级吸附动力学方程(式(5))进行拟合, 两种动力学模型的方程式分别如式(4)~(5)所示(Ho et al., 1999).
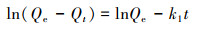
|
(4) |
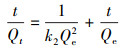
|
(5) |
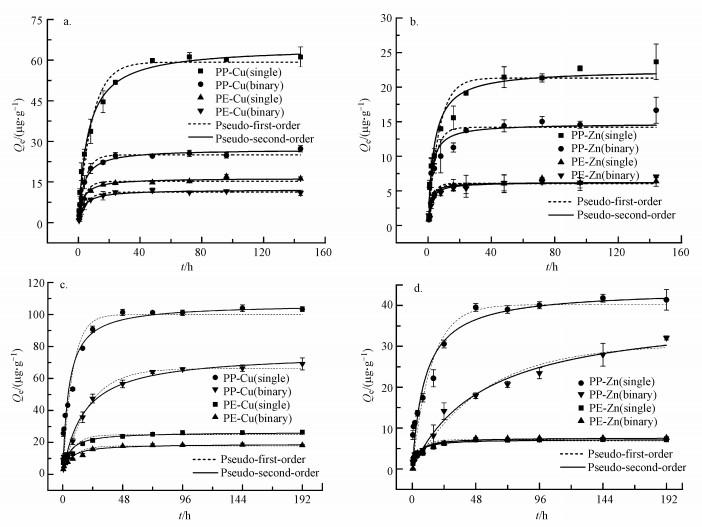 |
| 图 5 单一和二元重金属体系中virgin-MPs-Cu2+(a)、virgin-MPs-Zn2+(b)、aged-MPs- Cu2+(c)、aged-MPs-Zn2+(d)的吸附动力学拟合 Fig. 5 Adsorption kinetics fitting of virgin-MPs-Cu2+(a), virgin-MPs-Zn2+(b), aged-MPs- Cu2+(c) and aged-MPs-Zn2+(d) in single/binary heavy metal syste |
式中, Qe和Qt分别为MPs的平衡吸附量(μg·g-1)和在接触时间为t(min)时的吸附量(μg·g-1);k1和k2分别为拟一级(1/min)和拟二级(g·μg-1·min-1)吸附动力学的平衡速率常数.
由图 5分析得到, MPs对Cu2+和Zn2+的吸附过程在初期时吸附速率较高, 随着时间的延长, 吸附速率逐渐下降, 这可能是由于金属离子在吸附过程伊始快速迁移到微塑料表面, 而随后其吸附位点被占据导致扩散速率逐渐减缓所致(Fan et al., 2016).在单一体系中, MPs对重金属的吸附所需的平衡时间较短, 在48 h内即可达到吸附平衡, 而在二元体系中, 由于离子间竞争作用, 吸附质在吸附剂表面的扩散速度减慢, 导致所需平衡时间有所延长.不同微塑料老化前后进行对比分析可以发现, 老化后其对重金属离子的吸附能力得到增强, 以单一体系为例, 老化后PP、PE微塑料对Cu2+的吸附能力分别增长为原始微塑料的1.69、1.63倍(吸附量分别由59.26 μg·g-1增长为100.06 μg·g-1、15.24 μg·g-1增加到24.82 μg·g-1);老化后PP、PE微塑料对Zn2+的最大吸附量分别达到40.23 μg·g-1、6.85 μg·g-1, 分别为老化之前的1.91、1.14倍.紫外老化作用显著提升微塑料对重金属离子的吸附能力.原始微塑料的动力学拟合参数如表 2所示, 吸附过程更符合二级动力学模型.
| 表 2 原始微塑料对重金属离子的吸附动力学参数 Table 2 Adsorption kinetic parameters of heavy metal ions by original microplastics |
此外, 由图 5c~5d可知, 老化PP相比老化PE所需的平衡时间要长, 这是由于PP对金属离子的有效吸附位点更多, 因此达到吸附平衡需要时间更长(Deng et al., 2017).同时, MPs对复合体系中金属离子的吸附能力相比单一体系中有所下降, 这是由于Cu2+和Zn2+之间的离子竞争吸附作用(Huang et al., 2017).吸附动力学拟合参数如表 3所示, 微塑料对单一或复合体系中重金属Cu2+和Zn2+的吸附动力学过程更符合拟二级动力学模型, 其R2值均大于拟一级动力学模型中的R2值.
| 表 3 老化微塑料对重金属离子的吸附动力学参数 Table 3 Adsorption kinetic parameters of heavy metal ions by aged microplastics |
通过Langmuir吸附等温线模型(式(6))和Freundlich吸附等温线模型(式(7))来研究达到吸附平衡后重金属离子与吸附剂之间的相互作用关系.

|
(6) |
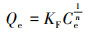
|
(7) |
式中, Qm为微塑料对重金属离子的单层吸附饱和吸附量(μg·g-1), KL为Langmuir常数(L·μg-1);Ce为溶液中重金属离子的平衡浓度(μg·L-1), KF为Freundlich吸附系数(μg·g-1);1/n为吸附强度或表面非均质性(L·g-1).
根据不同微塑料的吸附等温线(图 6), 分析可知, 紫外老化作用可以显著增强微塑料样品对重金属离子的吸附能力, 这可能与老化过程中微塑料物化性质的改变有关.此外, 重点分析老化后微塑料的吸附行为, 可以发现, 老化PP对两种重金属的吸附量均大于老化PE, 经分析得到, 由于PP的比表面积大于PE, 且PP受光照老化影响较大, 表面生成较多的含氧功能基团, 提高了其与金属之间的分子间作用力.同时发现, MPs对Cu2+的吸附量大于Zn2+, 这是由于两种金属离子的电负性和离子半径的差异导致, 其中Cu2+的电负性为28.56 eV≈Zn2+(28.84 eV), Cu2+的离子半径为0.72 A0, 小于Zn2+的离子半径(0.74 A0), 即Cu2+相比Zn2+具有较为接近的电负性和较小的离子半径, 使得Cu2+和MPs表面的静电引力作用较大, 从而使得对其吸附量增加(Huang et al., 2019).在复合体系中, 由于表面吸附位点的竞争吸附, 多价重金属离子的共存可以减少金属在非均质系统中的吸附(Fisher-Power et al., 2016), 使得金属离子的吸附量相比单一体系有所降低.MPs对金属离子的等温线拟合结果如表 4、5所示, 由R2值分析得到, 原始MPs对重金属的等温吸附过程复合Langmuir吸附模型, 而老化后微塑料的等温吸附过程与Freundlich等温线方程拟合度较高, 结果表明, 原始MPs对金属离子的吸附以单层的物理吸附为主, 而老化MPs对重金属离子吸附以多层吸附为主(Wang et al., 2018), 其中1/n的值均小于1, 进一步证明该吸附过程主要是非均质吸附过程.
 |
| 图 6 单一和二元重金属体系中不同微塑料对重金属的吸附等温线拟合(298 K) (a.virgin-MPs-Cu2+, b.virgin-MPs-Cu2+, c.virgin-MPs-Cu2+, d.virgin-MPs-Cu2+) Fig. 6 Adsorption isotherm fitting of virgin-MPs-Cu2+(a), virgin-MPs-Zn2+(b), aged-MPs- Cu2+(c) and aged-MPs-Zn2+(d)in single and binary heavy metal system at 298 K |
| 表 4 原始微塑料对重金属离子的等温吸附参数 Table 4 Adsorption isotherm parameters of heavy metal ions by original microplastics |
| 表 5 老化微塑料对重金属离子的吸附等温线参数 Table 5 Adsorption isotherm parameters of heavy metal ions by aged microplastics |
微塑料对重金属离子的吸附行为还受到温度的影响.热力学等温线主要用于评价吸附剂在吸附过程中能量和熵的变化.热力学吸附过程如式(8)~(9)所示.
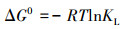
|
(8) |

|
(9) |
式中, ΔG0为自由能变化量(J·mol-1);ΔH0和ΔS0分别为焓(J·mol-1)和熵(J·mol-1·K-1);R为气体常数8.314 J·mol-1·K-1;T为绝对温度(K);KL为Langmuir常数(L·mol-1).
由图 7和图 8可知, 随着温度的升高, MPs对Cu2+和Zn2+的吸附能力明显增强.在试验温度为288~308 K的条件下, ΔG0计算为负值(表 6、表 7), 即吸附过程为自发反应过程, 且ΔG0的绝对值随着温度的升高而增大, 该结果表明, 随温度的升高, 吸附的自发反应程度增强.同时, 计算得到ΔH0为正值, 即表明该吸附过程是吸热反应, 这可能是由于金属离子去溶剂化所吸收的热量大于金属离子吸附到MPs表面所释放的热量(Godoy et al., 2019).ΔS0值也为正值, 说明固液界面的吸附过程向着无序化方向进行, 即金属离子与表面官能团的相互作用可能会改变MPs的结构(Wang et al., 2019).
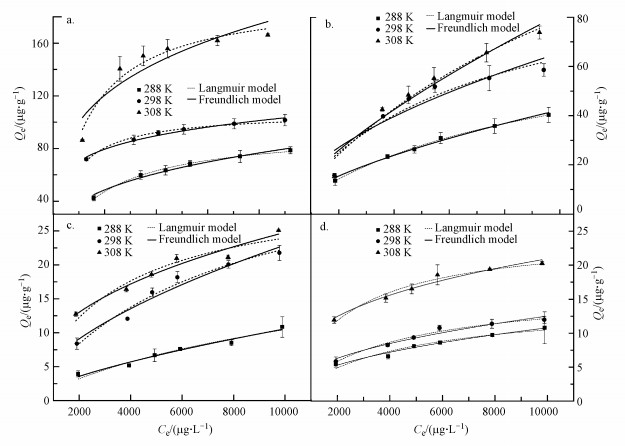 |
| 图 7 单一/二元体系中微塑料对Cu2+的吸附热力学 Fig. 7 Adsorption thermodynamic curves of Cu2+ onto PP in single metal ion solution(a), PP in binary metal ion solution(b), PE in single metal ion solution(b) and PE in binary metal ion solution(d) |
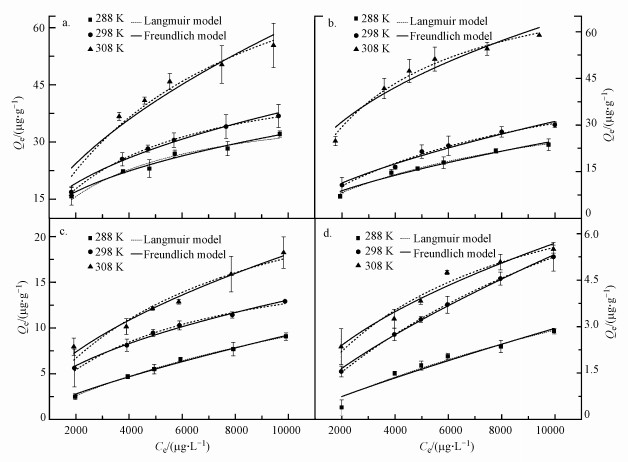 |
| 图 8 单一/二元体系中微塑料对Zn2+的吸附热力学 Fig. 8 Adsorption thermodynamic curves of Zn2+ onto PP in single metal ion solution(a); PP in binary metal ion solution(b); PE in single metal ion solution(c) and PE in binary metal ion solution(d) |
| 表 6 单一体系中微塑料对重金属离子的吸附热力学参数 Table 6 Thermodynamic parameters of Cu2+ and Zn2+ adsorption onto microplastics in single metal ion system |
| 表 7 二元体系中微塑料对重金属离子的吸附热力学参数 Table 7 Thermodynamic parameters of Cu2+ and Zn2+ adsorption onto microplastics in binary system |
通过考察溶液初始pH对两种MPs吸附Cu2+和Zn2+的影响, 结果如图 9所示.由于pH值影响了溶液中的金属形态, MPs表面电荷密度以及活性官能团的解离, 从而影响吸附剂的吸附行为.当pH值在3.0~6.0范围内时, 随着pH值的增加, MPs对重金属的吸附能力逐渐增强.由于在较低的pH值下, H+容易与金属离子产生竞争吸附作用, 占据MPs表面的吸附位点, 使得MPs对重金属离子的吸附能力下降, 而随着pH值的升高, H+竞争作用减弱, MPs的吸附量随之升高;同时, 在pH值较低时, MPs表面电荷较少, 而随着pH值的升高, 去质子化作用使得MPs上的功能基团更易与目标离子结合, 提高其吸附能力(Qiu et al., 2019).在二元体系中, pH值对吸附行为的影响结果与单金属体系相似.
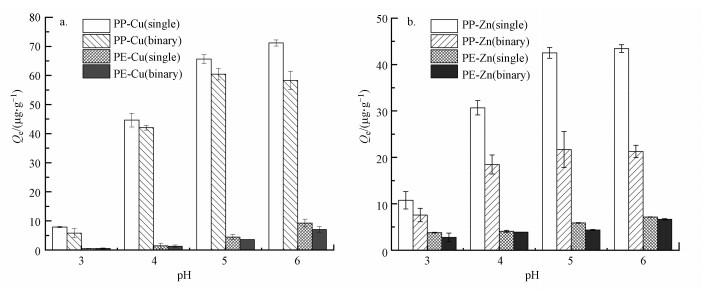 |
| 图 9 单一和二元重金属体系中pH值对老化微塑料吸附重金属Cu2+(a)和Zn2+(b)的影响 Fig. 9 Effect of pH on the adsorption of Cu2+(a) and Zn2+(b) by aged microplastics in single and binary system |
由于微塑料表面带有负电荷, 而重金属离子带有正电荷, 因此两者之间可以通过静电引力或形成络合物达到吸附的目的, 通过研究pH值对吸附能力的影响, 结果证明, pH值对微塑料吸附容量的影响作用较大, 即微塑料表面电荷的变化对吸附重金属能力影响较大, 进一步证明微塑料对重金属离子的吸附作用主要由于静电引力作用(Ashton et al., 2010;Brennecke et al., 2016).老化后的PP微塑料吸附两种重金属前后的SEM-EDS分析结果对比研究发现(图 10), 吸附前的微塑料表面没有检测到铜和锌的存在, 而吸附后微塑料表面检测有铜原子和锌原子, 即两种重金属被吸附在微塑料表面.进一步通过吸附前后的XPS的C1s峰比较分析(图 11), 结果发现, 经过老化后的PP和PE均产生了明显的C—O峰(285.3 eV), 经过吸附后C—O基团的结合能位置发生了偏移, 结合能增加, 有明显的失电子趋势, 电荷向正方向移动, 即—C—O作为供电子基团参与吸附反应(Dong et al., 2019).同时, 吸附后的含氧基团C—O基团的峰相对强度明显变小(图 11b), 有可能是含氧官能团与铜和锌发生反应生成金属氧化物, 占据了O的位点, 通过文献报道分析, Cu2+和Zn2+可以与老化后的微塑料表面的含氧官能基团反应生成相应的氧化物如CuO、Cu(OH)2和ZnO等沉积在微塑料表面导致的(Huang et al., 2019).
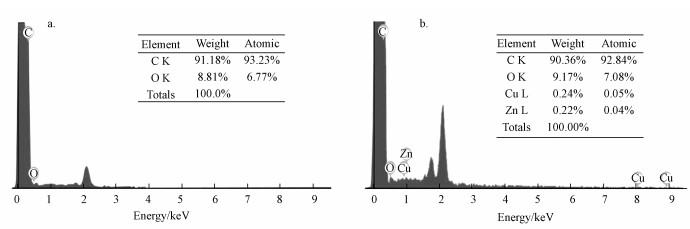 |
| 图 10 吸附重金属前后的老化PP和PE微塑料表面能谱分析 Fig. 10 EDS analysis of PP microplastics before (a) and after (b) adsorption of metal ions in the binary system |
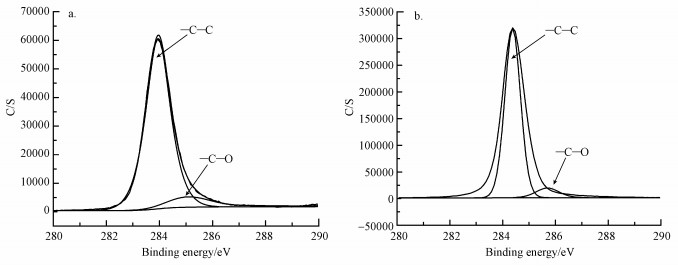 |
| 图 11 老化PP微塑料的C1s谱图分析 (a.吸附前, b.吸附后) Fig. 11 XPS spectrum showing the Peak value of C1s before(a) and after(b) adsorption by PP microplastics |
通过研究微塑料吸附前后FTIR谱图(图 12), 结果表明, 吸附重金属后的PP微塑料表面的—OH(3430 cm-1)发生了红移, 变化至3444.24 cm-1, 由文献报道得到, 重金属的吸附主要和吸附材料表面的含氧基团有关, 当微塑料吸附重金属后, 金属离子可能和氧发生络合作用, 导致—OH键长度的缩短, 进一步导致光谱吸收峰的红移(Dong et al., 2019).
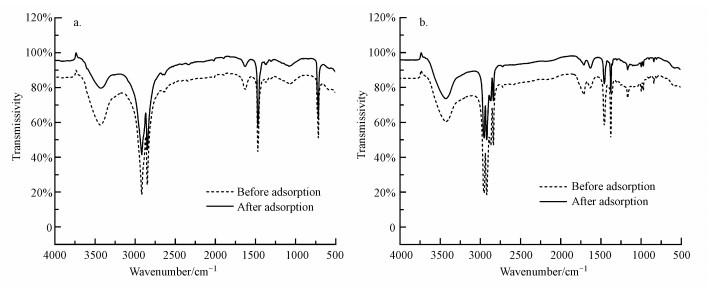 |
| 图 12 不同微塑料吸附前后的红外谱图 (a.PP, b.PE) Fig. 12 FTIR analysis of PP(a) and PE(b) microplastics before and after adsorption |
综合以上分析结果, 老化后的微塑料对重金属离子的吸附机理主要是依靠静电引力和含氧官能团的结合作用.
3.7 微塑料对藻类生长的影响微塑料对藻类的生长均有明显的抑制作用, 其中老化PP和PE与藻混合培养24 h后的抑制率分别为85.6%和76.5%, 主要是由于MPs在藻类光合作用过程中的遮蔽作用和MPs对营养物质的吸收(Wang et al., 2020).而随着培养时间的延长, 抑制率有所下降, 这是由于藻类在生长过程中的适应性和自我修复作用.而吸附金属离子(Cu2+/Zn2+)后的微塑料对藻类的生长抑制率明显低于单独微塑料的抑制作用.该结果表明, 负载微量金属离子浓度的微塑料可能导致对莱茵衣藻的生长抑制率下降, 其中Cu2+、Zn2+作为植物生长的营养元素, 可以一定程度上促进藻类的生长, 同时, 负载后的微塑料表面电荷的变化有可能也会影响微塑料与藻类之间的相互作用力.
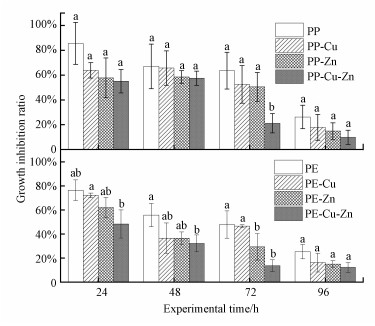 |
| 图 13 不同处理组对莱茵衣藻的生长抑制率 (不同的字母表示不同处理条件下存在显著性差异(p < 0.05)) Fig. 13 Effects of different treatments on the growth ratio of microalgae C. reinhardtii. (Data are expressed as means ± SD and values with different letters represent significant difference (p < 0.05) between treatments.) |
MDA酶活性指标是用来评估活性氧(ROS)对细胞造成的脂质过氧化损伤.此外, SOD和CAT的含量也反映了机体对ROS氧化损伤的抗氧化防御能力(Yang et al., 2020).从图 14可以看出, 微塑料处理后藻的MDA含量明显高于对照组, 即MPs存在时产生ROS, 这是导致藻产生氧化应激的原因(Bhattacharya et al., 2010).而MDA含量表明, 吸附金属离子的微塑料导致MDA含量显著低于单独微塑料存在下(p < 0.05), 结果表明, 单独使用PP和PE微塑料比MPs吸附金属离子后引起的氧化损伤更严重.莱茵衣藻的SOD和CAT活性也显示出类似的趋势, 不同处理96 h后的SOD和CAT含量顺序为Control < MPs-Cu-Zn < MPs-Cu ≈ MPs-Zn) < MPs, 综合来看, 微塑料存在下对藻类有明显的毒性作用, 其中负载Cu或/和Zn的老化PP和PE的毒性明显低于单独的老化MPs.
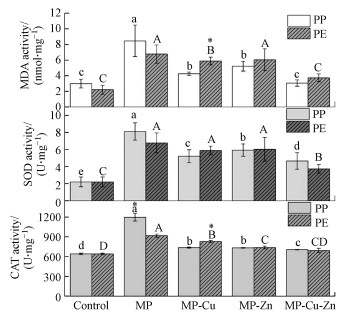 |
| 图 14 不同处理组对莱茵衣藻的酶活性的影响 (不同的符号表示不同处理条件下存在显著性差异(p < 0.05), 其中大写和小写字母分别代表PP和PE处理组间的显著性差异, (*)代表PP和PE处理组之间的差异.) Fig. 14 The activity of MDA, SOD and CAT in Chlamydomonas reinhardtii after different treatments.(Data are expressed as means ± SD. Differences for each treatment were noted with lowercase letters (PP treatment) or capital letters (PE treatment). Significant differences (p < 0.05) between PP and PE adsorbed with the same metal ions were noted with an asterisk (*)) |
本论文主要研究了紫外老化后的PP和PE微塑料对重金属离子Cu2+和Zn2+在单一和二元复合体系中的吸附行为, 通过吸附动力学拟合模型研究得到, Zn2+和Cu2+在单一和竞争体系中的吸附过程均符合拟二级动力学模型, 其中在单一体系中吸附速率较快, 而在复合体系中受竞争吸附的影响, 使膜扩散速率减慢, 同时对Cu2+的选择性较强.吸附等温线拟合研究发现, 老化PP由于其比表面积大, 含氧功能基团较多, 对金属离子的吸附能力高于老化PE, 其中对Cu2+的吸附量大于Zn2+, 两种体系中MPs对金属离子的吸附行为均更符合Freundlich模型, 由于二元体系中的金属离子对活性位点的竞争吸附作用, 导致MPs对金属离子的吸附量有所下降.吸附热力学结果表明, 吸附过程为自发的吸热反应过程, 且随着温度的升高, 吸附的自发反应程度增强.pH值对MPs吸附重金属影响结果表明, 随着pH值的增加, MPs对重金属的吸附能力逐渐增强, 这是受到溶液中氢离子的竞争吸附作用和吸附剂表面带电性等的影响. 通过微塑料表面官能基团的变化分析结果得到, 老化后微塑料对重金属的吸附作用主要是受到静电引力和含氧官能团的结合作用影响.进一步分析了藻的生长抑制率和酶活性的变化来研究吸附重金属前后的微塑料对藻的毒性效应影响, 结果表明, 微塑料存在下对藻的生长有明显的抑制作用, 其中吸附了微量重金属Cu2+和Zn2+的微塑料对藻的毒性作用有明显减弱.本研究为研究微塑料在多元重金属离子污染物体系中的环境行为以及MPs与其他污染物共存条件下对在水生生态效应的影响提供了理论依据.
Ashton K, Holmes L, Turner A. 2010. Association of metals with plastic production pellets in the marine environment[J]. Marine Pollution Bulletin, 60(11): 2050-2055. DOI:10.1016/j.marpolbul.2010.07.014 |
Bellingeri A, Bergami E, Grassi G, et al. 2019. Combined effects of nanoplastics and copper on the freshwater alga Raphidocelis subcapitata[J]. Aquatic Toxicology, 210: 179-187. DOI:10.1016/j.aquatox.2019.02.022 |
Bhattacharya P, Lin S J, Turner J, et al. 2010. Physical adsorption of charged plastic nanoparticles affects algal photosynthesis[J]. The Journal of Physical Chemistry C, 114(39): 16556-16561. DOI:10.1021/jp1054759 |
Brennecke D, Duarte B, Paiva F, et al. 2016. Microplastics as vector for heavy metal contamination from the marine environment[J]. Estuarine Coastal and Shelf Science, 178: 189-195. DOI:10.1016/j.ecss.2015.12.003 |
Browne M A, Crump P, Niven S J, et al. 2021. Accumulation of microplastic on shorelines worldwide: Sources and sinks[J]. Environmental Science & Technology, 45(21): 9175-9179. |
Calderon B, Fullana A. 2015. Heavy metal release due to aging effect during zero valent iron nanoparticles remediation[J]. Water Research, 83(oct.15): 1-9. |
Canniff P M, Hoang T C. 2018. Microplastic ingestion by Daphnia magna and its enhancement on algal growth[J]. Science of the Total Environment, 633: 500-507. DOI:10.1016/j.scitotenv.2018.03.176 |
Cole M, Lindeque P, Halsband C, et al. 2011. Microplastics as contaminants in the marine environment: A review[J]. Marine Pollution Bulletin, 62(12): 2588-2597. DOI:10.1016/j.marpolbul.2011.09.025 |
Connors K A, Dyer S D, Belanger S E. 2017. Advancing the quality of environmental microplastic research[J]. Environmental Toxicology and Chemistry, 36(7): 1697-1703. DOI:10.1002/etc.3829 |
Deng J, Liu Y, Liu S, et al. 2017. Competitive adsorption of Pb(Ⅱ), Cd(Ⅱ) and Cu(Ⅱ) onto chitosan-pyromellitic dianhydride modified biochar[J]. Journal of Colloid and Interface Science, 506: 355-364. DOI:10.1016/j.jcis.2017.07.069 |
Dong Y, Gao M, Song Z, et al. 2019. As(Ⅲ) adsorption onto different-sized polystyrene microplastic particles and its mechanism-ScienceDirect[J]. Chemosphere, 239: 124792-124792. |
Dong Y, Gao M, Song Z, et al. 2019. Adsorption mechanism of As(Ⅲ) on polytetrafluoroethylene particles of different size[J]. Environmental Pollution, 254(Pt A): 112950. |
Fan C Z, Li K, Li J X, et al. 2016. Comparative and competitive adsorption of Pb(Ⅱ) and Cu(Ⅱ) using tetraethylenepentamine modified chitosan/CoFe2O4 particles[J]. Journal of Hazardous Materials, 326: 211-220. |
Fisher-Power L M, Cheng T, Rastghalam Z S. 2016. Cu and Zn adsorption to a heterogeneous natural sediment: Influence of leached cations and natural organic matter[J]. Chemosphere, 144: 1973-1979. DOI:10.1016/j.chemosphere.2015.10.109 |
Godoy V, Martin-Lara M A, Calero M, et al. 2019. Physical-chemical characterization of microplastics present in some exfoliating products from Spain[J]. Marine Pollution Bulletin, 139: 91-99. DOI:10.1016/j.marpolbul.2018.12.026 |
Gewert B, Plassmann M, MacLeod M. 2015. Pathways for degradation of plastic polymers floating in the marine environment[J]. Environmental Science-Processes & Impacts, 17(9): 1513-1521. |
Ho Y S, McKay G. 1999. Pseudo-second order model for sorption processes[J]. Process Biochemistry, 34(5): 451-465. DOI:10.1016/S0032-9592(98)00112-5 |
Holmes L A, Turner A, Thompson R C. 2012. Adsorption of trace metals to plastic resin pellets in the marine environment[J]. Environmental Pollution, 160: 42-48. DOI:10.1016/j.envpol.2011.08.052 |
Holmes L A, Turner A, Thompson R C. 2014. Interactions between trace metals and plastic production pellets under estuarine conditions[J]. Marine Chemistry, 167: 25-32. DOI:10.1016/j.marchem.2014.06.001 |
Hodson M E, Duffus-Hodson C A, Clark A, et al. 2017. Plastic bag derived-microplastics as a vector for metal exposure in terrestrial invertebrates[J]. Environmental Science and Technology, 51(8): 4714-4721. DOI:10.1021/acs.est.7b00635 |
Huang B, Wei Z B, Yang L Y, et al. 2019. Combined toxicity of silver nanoparticles with hematite or plastic nanoparticles toward two freshwater algae[J]. Environmental Science & Technology, 53(7): 3871-3879. |
Huang X N, Zemlyanov D Y, Diaz-Amaya S, et al. 2019. Competitive heavy metal adsorption onto new and aged polyethylene under various drinking water conditions[J]. Journal of Hazardous Materials, 385: 121585. |
Huang X N, Zhao S, Abu-Omar M, et al. 2017. In-situ cleaning of heavy metal contaminated plastic water pipes using a biomass derived ligand[J]. Journal of Environmental Chemical Engineering, 5(4): 3622-3631. DOI:10.1016/j.jece.2017.07.003 |
Lin L, Zuo L Z, Peng J P, et al. 2018. Occurrence and distribution of microplastics in an urban river: A case study in the Pearl River along Guangzhou City, China[J]. Science of the Total Environment, 644: 375-381. DOI:10.1016/j.scitotenv.2018.06.327 |
李文华, 简敏菲, 刘淑丽, 等. 2020. 鄱阳湖湖口-长江段沉积物中微塑料与重金属污染物的赋存关系[J]. 环境科学, 41(1): 242-252. |
Ma Y, Huang A, Cao S, et al. 2016. Effects of nanoplastics and microplastics on toxicity, bioaccumulation, and environmental fate of phenanthrene in fresh water[J]. Environmental Pollution, 219: 166-173. DOI:10.1016/j.envpol.2016.10.061 |
Prata J C, Costa J P, Lopes I, et al. 2019. Effects of microplastics on microalgae populations: A critical review[J]. Science of the Total Environment, 665: 400-405. DOI:10.1016/j.scitotenv.2019.02.132 |
Prata J C, Reis V, Pao A, et al. 2019. Effects of spatial and seasonal factors on the characteristics and carbonyl index of (micro)plastics in a sandy beach in Aveiro, Portugal[J]. Science of the Total Environment, 709: 135892. |
Qiu H, Ni W X, Zhang H, et al. 2019. Fabrication and evaluation of a regenerable HFO-doped agricultural waste for enhanced adsorption affinity towards phosphate[J]. Science of the Total Environment, 703: 135493. |
Thompson R C, Olsen Y, Mitchell R P, et al. 2004. Lost at sea: Where is all the plastic[J]. Science, 304(5672): 838-838. DOI:10.1126/science.1094559 |
Wagner M, Scherer C, Alvarez-Muñoz D, et al. 2014. Microplastics in freshwater ecosystems: what we know and what we need to know[J]. Environmental Sciences Europe, 26(1): 1-9. DOI:10.1186/2190-4715-26-1 |
Wang F Y, Yang W W, Cheng P, et al. 2019. Adsorption characteristics of cadmium onto microplastics from aqueous solutions[J]. Chemosphere, 235: 1073-1080. DOI:10.1016/j.chemosphere.2019.06.196 |
Wang Q J, Wangjin X, Zhang Y, et al. 2020. The toxicity of virgin and UV-aged PVC microplastics on the growth of freshwater algae Chlamydomonas reinhardtii[J]. Science of the Total Environment, 749: 141603. DOI:10.1016/j.scitotenv.2020.141603 |
Wang Q J, Zhang Y, Wang J X, et al. 2020. The adsorption behavior of metals in aqueous solution by microplastics effected by UV radiation[J]. Journal of Environmental Sciences, 87: 272-280. DOI:10.1016/j.jes.2019.07.006 |
Wang W F, Wang J. 2018. Comparative evaluation of sorption kinetics and isotherms of pyrene onto microplastics[J]. Chemosphere, 193: 567-573. DOI:10.1016/j.chemosphere.2017.11.078 |
Wu Y, Guo P, Zhang X, et al. 2019. Effect of microplastics exposure on the photosynthesis system of freshwater algae[J]. Journal of Hazardous Materials, 374: 219-227. DOI:10.1016/j.jhazmat.2019.04.039 |
薛向东, 王星源, 梅雨晨, 等. 2020. 微塑料对水中铜离子和四环素的吸附行为[J]. 环境科学, 41(8): 3675-3683. |
Yang J, Cang L, Sun Q, et al. 2019. Effects of soil environmental factors and UV aging on Cu2+ adsorption on microplastics[J]. Environmental Science and Pollution Research, 26(22): 23027-23036. DOI:10.1007/s11356-019-05643-8 |
Yang W F, Gao X X, Wu Y X, et al. 2020. The combined toxicity influence of microplastics and nonylphenol on microalgae Chlorella pyrenoidosa[J]. Ecotoxicology and Environmental Safety, 195: 110484. DOI:10.1016/j.ecoenv.2020.110484 |
张子琪, 高淑红, 康园园, 等. 2020. 中国水环境微塑料污染现状及其潜在生态风险[J]. 环境科学学报, 40(10): 3574-3581. |
周泽妍, 王思琦, 张盼月, 等. 2021. 白洋淀-府河入淀口段沉积物中微塑料的丰度及分布特征[J]. 环境工程学报, 15(1): 360-367. |
Zhu Z L, Wang S C, Zhao F F, et al. 2019. Joint toxicity of microplastics with triclosan to marine microalgae Skeletonema costatum[J]. Environmental Pollution, 246: 509-517. DOI:10.1016/j.envpol.2018.12.044 |
 2021, Vol. 41
2021, Vol. 41