2. 中国电建集团华东勘测设计研究院有限公司, 杭州 310000
2. PowerChina Huadong Engineering Corporation Limited, Hangzhou 310000
近年来, 随着科学技术的发展和全球能源产业结构调整变化, 高效、清洁、经济的核能进入了快速发展时期, 但随之产生的核污染事件和核废物也亟待解决(van der Merwe, 2019; Zhang et al., 2020).放射性核素会对土壤和水环境产生极为不利的影响, 其中, 137Cs作为主要放射源具有半衰期长、溶解性强的高危害性, 对人体造成更高的健康风险(Aoyama, 1988; Yang et al., 2011; Querfeld et al., 2019).从环保和可持续发展角度而言, 开发新技术和新材料提取放射性废水中137Cs具有重要的现实意义(Chen et al., 2020).当前去除137Cs的主要方法为沉淀法、固定化法、萃取和离子交换法(蔡璇等, 2012).因具有成本相对较低、易于操作等优点, 离子交换和吸附法成为国内外研究热点(Klaysom et al., 2011).这其中, 研发制备高吸附量、高选择性、结构稳定的环境友好型吸附材料(徐世平等, 2000)已成为去除和富集放射性废水中137Cs的关键.
目前, 已经研究制备的有机和生物材料在高温、高辐射环境下大多存在易降解、再生困难等问题.与此相比, 无机离子交换吸附剂因具有较高的稳定性和出色的吸附性能而成为备受青睐的除137Cs材料(Clarke et al., 1998).虽然许多天然材料(高岭土、蒙脱土、沸石等)和化学合成材料(多价金属磷酸盐、金属亚铁氰化物等)可以在中性或者碱性条件下从水溶液中去除Cs+, 但杂多酸盐阳离子交换剂在高酸性介质中对Cs+仍具有很好的吸附性能, 且对Cs+吸附特异性高、吸附动力学良好(Tranter et al., 2002).无机离子交换剂磷钼酸铵(AMP), 化学式为(NH4)3PMo12O4·H2O, 作为杂多酸盐类的一种具有独特的Keggin结构, 根据Smit(1958)的相关研究可知, [PMo12O40]3-是由12个MoO3八面体组成的空心球, 具体结构分解为:每3个MoO3共用一个O原子, 组成Mo3O10的基本结构单元, 4个基本单元组成一个空心球的基础结构, PO43-基团位于该球结构的中心位置, 形成了由多个多面体堆积的空间网络, 有大量的空隙, 这对于吸附剂是良好的结构形态.Buchwald和Thistlethwaite基于晶格中Cs+与NH4+的同构交换, 提出了AMP的离子交换机制, 他们认为[PMo12O40]3-阴离子的穴状四面体错综复杂的贯通间隙之中缔合了可以与Cs+置换的NH4+, 从而达到离子交换吸附Cs+的目的(Buchwald et al., 1958).
虽然AMP因其在高酸环境下对Cs+的高选择性和高离子交换容量已被认为是良好的除铯(Cs+)材料, 但由于其微晶结构和细粉形态导致吸附后难以分离等问题(Ye et al., 2009), 许多研究致力于用水力性能好的载体基质固定AMP粉末, 如聚丙烯腈(Holdsworth et al., 2019)、二氧化硅(Dan et al., 2019)和氧化铝(Chakravarty et al., 2012)等, 但这些材料大多存在耐酸碱性较差、吸附效率较低、合成较复杂等问题.已有研究发现, 聚乙烯醇(PVA)是应用广泛的水溶性高分子聚合物, 含有大量羟基和极强的氢键, 具有良好的热稳定性和机械强度等优点(Hassan et al., 2000), 可改善AMP的水力学性能, 提高其在柱实验操作中的稳定性, 便于实际应用.同时引入良好的多孔硅胶TEOS与PVA杂化形成具有特定网络结构的基质, 其网状限制效应可以获得优良的介孔或者微孔结构, 为AMP的复合带来尽可能多且尺寸合适的空间, 从而为Cs+提供更多的吸附位点(Deng et al., 2016).二者对AMP均具有较好的包埋效果和一定的吸附能力, 因此, 可将其作为AMP复合材料的基质载体.此外, 添加经过TEOS的功能化修饰的纳米Fe3O4可用于分离溶液中AMP复合材料与Cs+.
基于此, 本研究采用溶胶-凝胶共沉淀法将AMP包埋于PVA-TEOS多孔基质中, 以优化AMP离子交换的吸附性能, 增强其在高酸性介质中的耐水性和稳定性, 制备除Cs+性能优良的复合材料.同时, 采用多种手段表征材料的形态结构和吸附特性, 探究其对水溶液中Cs+的去除性能和机理.
2 材料与方法(Materials and methods) 2.1 试验材料钼酸铵、聚乙烯醇、正硅酸四乙酯、碳酸钠、磷酸、硝酸、四水合氯化亚铁、六水和氯化铁、氨水(25%)均为分析纯, 购于国药集团化学试剂有限公司;CsCl为光谱纯, 购于美国Amresco公司;实验用水为去离子水.
2.2 材料的制备 2.2.1 AMP的制备称取0.93 g的(NH4)6Mo7O24·4H2O溶于10 mL去离子水中, 待完全溶解后向溶液中缓慢滴加2 mL 0.25 mol·L-1的H3PO4, 边添加边搅拌;在70 ℃恒温下逐滴添加0.5 mL 6 mol·L-1的HNO3调节混合溶液的pH, 直至出现黄色沉淀, 并继续搅拌0.5 h后静止陈化;过滤得到沉淀物, 用1 mol·L-1的HNO3溶液洗涤3次, 去离子水洗涤1次后过滤得到沉淀, 在(40±1) ℃烘箱内干燥, 可制得黄色粉末状AMP.
2.2.2 纳米磁性Fe3O4制备将浓度为0.5 mol·L-1的FeCl2·4H2O和FeCl3·6H2O溶液以物质的量比1:2混合, 在N2保护下室温搅拌15 min.量取0.25 mol·L-1物质的量为总铁离子3倍的NH3·H2O迅速加入到混合液中并恒温90 ℃搅拌反应1 h, 冷却至室温;将合成的黑色沉淀物进行磁分离得到磁流体即为纳米磁性Fe3O4.最后置于400 mL去离子水中保存备用.
2.2.3 磷钼酸铵/聚乙烯醇颗粒(AMP-PVA)的制备分别称取0.5~3.0 g不同质量的Na2CO3粉末掺杂到溶解有5.0 g PVA的80 mL去离子水中, 在90 ℃沸水浴中加热搅拌2 h直至相互溶解;接着加入10 mL纳米磁性Fe3O4, 搅拌均匀后加入5 mL NH3·H2O, 再缓慢加入3 mL TEOS搅拌5 h;最后加入15 g AMP粉末, 继续搅拌12 h, 最后得到均一的溶胶.将溶胶至于室温下冷却, 加入0.5 mol·L-1的HCl溶液, 待完全反应后将其放入冷冻干燥机中干燥, 即可得到多孔磷钼酸铵/聚乙烯醇材料(AMP-PVA).最后将其切割成微米级三维结构颗粒, 封装室温保存.
2.3 材料的表征通过扫描电子显微镜/能谱(SEM-EDX, S-4800/EX-350, 日本)对AMP、吸附前后的AMP-PVA颗粒进行形态样貌分析, 用于表征吸附剂改性前后及吸附前后形貌变化及其表面元素成分定性定量分析;利用傅里叶红外光谱(FTIR, Affinity-1, 日本)分析AMP、吸附前后AMP-PVA颗粒结构中官能团类型及含量的变化;对吸附前后的AMP-PVA颗粒进行X射线光电子能谱(XPS, ESCSLAB, 美国)分析, 测定其吸附前后各元素的电子结合能的变化;利用X射线衍射仪(XRD, D8 ADVANCE, 德国)分析AMP和AMP-PVA颗粒的晶体结构及物相;利用N2吸附脱附等温线(BET, ASAP2460, 美国)分析不同原料掺杂情况下AMP-PVA的比表面积、孔容、孔径大小;利用热重分析仪(TG-DSC, SDT Q600, 美国)测定AMP、AMP-PVA的热稳定性.
2.4 吸附实验配制50 mL所需溶液加入到100 mL锥形瓶中, 称取0.05 g的AMP-PVA颗粒加入到上述溶液中, 调节溶液pH、温度、时间等参数, 每组设置3个平行样, 恒温振荡后用0.45 μm滤膜进行过滤, 使用ICP-MS测定所得上清液中的Cs+浓度, 可定量确定AMP-PVA颗粒对Cs+的吸附效果.分别考察pH(2~12)、时间(0.5~48 h)、初始Cs+浓度(10~200 mg·L-1)、吸附温度(15、25、35 ℃)对吸附效果的影响, 并研究AMP-PVA的吸附动力学和热力学特性.吸附量计算公式如下:

|
(1) |
式中, qe为Cs+的平衡吸附容量(mg·g-1);C0为溶液中的Cs+初始浓度(mg·L-1);Ce为吸附平衡时的Cs+浓度(mg·L-1);m为吸附剂添加量(g);V为溶液添加量(L).
3 结果与讨论(Results and discussion) 3.1 AMP-PVA颗粒对Cs+的吸附性能 3.1.1 初始Cs+浓度对吸附效果的影响在不同温度条件下, Cs+初始浓度(C0)对AMP-PVA颗粒吸附效果的影响如图 1a所示, 实验条件为C0=0~220 mg·L-1, pH=7.7, 反应时间15 h.由图 1a可知, 在初始浓度C0为0~75 mg·L-1范围内, AMP-PVA颗粒对Cs+的吸附量随着浓度的升高而呈现线性增加的关系;当初始浓度C0在75~125 mg·L-1时吸附量随着初始浓度的增加缓慢增加;而初始浓度C0>125 mg·L-1时, 吸附曲线变得平缓直至不再增加.引起初始浓度效应的原因主要有两方面, 首先随着溶液浓度的增加, Cs+与材料表面碰撞几率更大, 更容易向吸附剂表面扩散, 被吸附活性位点吸引(Zong et al., 2017);另一方面, 由于反应进行程度和阶段不同引起Cs+拥有不同的反应行为, 低浓度时材料的表面活性位点数量远高于Cs+的数量, Cs+能够被充分吸附因而呈现线性关系, 而当浓度进一步增加, 离子数量增加使得材料的吸附位点逐渐饱和, 材料表面被离子包围很难有多余的空隙与其他Cs+接触, 吸附行为变得困难因而呈现出非线性趋势(饶本强等, 2020).
 |
| 图 1 不同温度下初始Cs+浓度(a)及不同pH(b)对AMP-PVA吸附Cs+的影响 Fig. 1 Effect of different Cs+ initial concentration and temperature(a) and different pH(b) on the adsorption capacity of AMP-PVA |
在实验条件下, 15、25、35 ℃时AMP-PVA的最大吸附量分别为70.10、72.10和75.65 mg·g-1, 说明随着温度的升高, AMP-PVA颗粒的最大吸附量也会有所增加.此外, 比较3个不同温度下的吸附曲线发现, 温度对吸附量随初始浓度变化的影响并不显著;随着初始浓度的升高, AMP-PVA在15 ℃时的吸附曲线要比35 ℃更早趋于平缓, 这是由于在35 ℃下, 溶液中分子的热运动更加剧烈使其扩散速率增加, 增大了与吸附位点的碰撞机会(Zhou et al., 2014).
3.1.2 pH对吸附效果的影响图 1b为不同pH条件下AMP-PVA颗粒吸附量的变化曲线, 实验条件为C0=100 mg·L-1, 反应温度25 ℃, 反应时间15 h.由图 1b可知, 由于AMP具有良好的耐酸性能(Park et al., 2013), 因而在pH=2~6时, 材料的吸附性能未有大幅波动.随着pH升高, 溶液逐渐变为中性, AMP-PVA颗粒对Cs+的吸附量也随之增加, 当pH=7.7时达到最大值53.52 mg·g-1, 这是由于溶液中H+的减少削弱了其与Cs+对吸附位点的竞争.当溶液pH增大为8~11, 呈现弱碱性时, Cs+仍以水合离子[Cs(H2O)n]+的形态呈现, 但由于Na+调节pH的引入与Cs+产生竞争占据部分位点, 吸附量随之降低, 当溶液pH=12及以上时, AMP极易与OH-发生化学反应(式(2)), 结构遭到破坏, 材料被溶解失去其大部分吸附功能.在实际应用中, 由于核反应堆中乏核燃料的PUREX/REDOX工艺处理及工业辐照器中对137Cs的处理都涉及到酸溶液, 因此, 含有放射性核素的污染水大多呈现强酸性或酸性(Tranter et al., 2002b; Anerjee et al., 2008), 从这一现象而言, 材料在强酸性条件下的良好性能更具有实际应用价值.
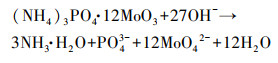
|
(2) |
图 2分别为Na2CO3添加量为0.5、1.0、1.5、2.0、2.5、3.0 g条件下合成的AMP-PVA复合材料的数码图像.从图 2中可以观察到, 随着Na2CO3添加量的增加, AMP-PVA复合材料颜色逐渐加深, 颗粒形态更明显.
 |
| 图 2 不同Na2CO3添加量合成的AMP-PVA图像 Fig. 2 AMP-PVA synthesized with different quality Na2CO3 |
图 3为掺杂不同质量Na2CO3的复合材料AMP-PVA在N2氛围下的等温吸附-脱附曲线.根据IUPAC分类标准, 等温线属于IV型, H3(H4)型滞后环, 没有明显的饱和吸附平台, 表明结构很不规整, 被认为是片状粒子堆积形成的狭缝、裂缝和楔形结构.从图 3中可以看出, 在低压段吸附量平缓增加, 此时N2分子以单层到多层吸附在介孔的内表面, 在P/P0 =0.45~1.0左右吸附量有一突增, 这一阶段反映了孔径的大小和均一性(Rojas et al., 2002).从孔径分布图可以得出, 复合材料的孔径分布不均匀, 微孔和介孔均有出现, 且在不同掺杂比中表现的百分比也不相同.从图中可以看出, 在添加量为0.5 g时孔径主要分布在4 nm左右, 以微孔为主要分布;而在添加量为1.0、1.5、2.0、2.5、3.0 g时, 由于孔径分布图纵坐标的差异, 在4 nm左右位置出现的峰值与5 nm以后的分布值相差不大, 说明其呈现为微孔和介孔多样性分布的特征.综合分析可知, Na2CO3的添加在一定范围内有助于材料多孔特性的形成.
 |
| 图 3 不同Na2CO3添加量合成的AMP-PVA的吸脱附曲线和孔径分布 Fig. 3 Adsorption and desorption behavior and the pore size distribution of different AMP-PVA |
图 4所示为不同Na2CO3添加量对复合材料孔径、孔容、比表面积及吸附Cs+的影响.从图 4a中可以看出, 不同Na2CO3添加量对吸附效果影响显著, 添加量从0.5 g逐渐增加到1.5 g时, 固液比(g·L-1)为1:1时吸附量略有增加, 而在固液比为1:2时吸附效果却有下降, 可能是由于溶液中Cs+的含量不足以使过量的拥有丰富多孔的APM-PVA颗粒达到吸附饱和, 材料已经达到吸附溶液中Cs+的临界值.因此, 在实际应用时要考虑溶液中Cs+的含量决定其吸附材料的投加量.对比图 4b中材料的开孔特性在添加量0.5~1.5 g范围内的改变符合其吸附效果的变化情况, 比表面积和孔容逐渐减小导致平均孔径逐渐增大, 使Cs+可以有更大的可能性进入到AMP内部与NH4+产生离子交换, 进而提高吸附效果.当Na2CO3的添加量超过1.5 g时, 吸附效果逐渐下降, 直至3.0 g时有部分提升, 对比分析不同添加量下的孔径特征和吸脱附曲线发现平均孔径的降低成为影响材料吸附效果的主要原因, 同时也发现在添加量为2.5 g时平均孔径却有所增加, 是因为其在50 nm左右仍有孔径分布, 这说明孔径过大的介孔和大孔分布会造成Cs+流失, 降低其吸附效果.
 |
| 图 4 不同Na2CO3添加量合成的AMP-PVA材料的吸附量变化(a)和结构特性(b) (实验条件:C0=100 mg·L-1, pH=7.7, 反应温度25 ℃, 反应时间15 h) Fig. 4 Change of adsorption capacity(a) and structural characteristics(b) of AMP-PVA synthesized with different amount of Na2CO3 |
AMP-PVA材料结构复杂, 其中, 吸附效果较好的是Na2CO3添加量为0.5、1.0和1.5 g的复合材料.综合分析图 2~4中3种材料的不同外貌形态、开孔特征, 考虑到材料实际应用时的耐水性和稳定性, 比较后选取形态呈现颗粒状, 孔径、比表面积和孔容分布最为均匀且吸附量相对较高的Na2CO3添加量为1.0 g的材料.
根据Flory-Krigbaum理论, 聚合物PVA链相互重叠形成交联网状结构(Flory et al., 1950).如图 5所示, 添加Na2CO3是为了调节聚合物PVA网状结构中网眼尺寸, 使其能够与TEOS水解产生的二氧化硅合成优良的多介孔PVA-SiO2基质.TEOS与PVA的缩合反应和酯交换反应均可以生成Si—O—C共价键, 以及PVA自身羟基形成的氢键均为多孔网状基质的交联点用于复合AMP细小颗粒, 影响AMP结晶的大小和尺寸, 进而影响其吸附能力(Deng et al., 2017).与此同时, TEOS在纳米Fe3O4颗粒表面形成核层结构负载于PVA-TEOS基质中, 基质负载的AMP的结晶过程吸引了Fe3O4纳米粒子并使其均匀镶嵌在其中, 但由于纳米Fe3O4颗粒包裹了无机材料使其饱和磁化强度降低.
 |
| 图 5 材料合成过程中结构变化 Fig. 5 Structure change in the process of material synthesis |
吸附动力学主要用于测定吸附过程中物理化学反应的速率, 探究吸附性能的控制步骤.本研究分别利用Lagergren准一级动力学方程(式(3))、Ho准二级动力学方程(式(4))、Weber-Morris颗粒内扩散模型(式(5))、Boyd外扩散速率控制模型(式(6))进行拟合.

|
(3) |

|
(4) |
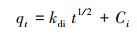
|
(5) |

|
(6) |
式中, k1为准一级动力学模型的吸附速率常数(h-1);k2为准二级动力学模型的吸附速率常数(g·mg-1·h-1);qe和qt分别为平衡时和时间t内吸附剂对溶液中Cs+的吸附容量(mg·g-1);kdi为模型中各环节的吸附速率常数(mg·g-1·min-0.5或mg·g-1·h-0.5);Ci为固体吸附剂边界层对各阶段反应速率影响程度(mg·g-1);F为在t时刻的吸附转换率;Bt为F的数学函数.
利用准一级动力学和准二级动力学模型(图 6a)、颗粒内扩散模型(图 6b)、Boyd外扩散速率控制模型(图 6c)对实验结果进行拟合, 拟合参数如表 1所示.通过比对4个模型的拟合结果, 发现准一级动力学和准二级动力学的拟合效果都较好(R2> 0.96).但准一级动力学模型通常只是用于吸附初始阶段的动力学描述, 而准二级动力学可综合反映液膜扩散、表面吸附和颗粒内扩散等吸附动力学机制(耿旭等, 2017).如图 6a所示, 在初始阶段溶液中的Cs+吸附量增加缓慢, 表明在该阶段吸附速率受液膜扩散控制即发生了外部的传质步骤, 这符合准一级动力学方程拟合结果.准二级动力学方程的拟合结果表明该反应过程受到吸附位的影响较大(黄园英等, 2019), 说明该吸附阶段Cs+吸附受颗粒内扩散的控制, 且以化学吸附为主.而内扩散模型和Boyd模型的拟合结果可以更好地论证复杂的吸附过程.图 6c显示, Boyd一级动力学拟合效果最好, R2=0.9875, 截距c=-0.111956, 曲线未经过原点, 表明该吸附过程为受液膜扩散、颗粒内扩散共同影响的化学吸附过程(黄召亚等, 2013).图 6b所示为Weber-Morris内部扩散分段线性拟合, 由表 1可知, 该内部扩散过程主要分为4个阶段, 每个阶段的截距都不为0, 说明该吸附过程不受内扩散的唯一控制, 与Boyd模型的拟合结果相符(梁成强等, 2019).此外, 第1阶段的吸附拟合效果较差(R2=0.7946), 说明初始过程受内扩散控制程度较低, 主要受到液膜阻力的影响, 且斜率较小, Kd1=1.387 mg·g-1·h-0.5, 吸附进程缓慢;吸附主要集中在第2阶段, Kd2=18.056 mg·g-1·h-0.5, 拟合效果较好(R2=0.9859), 表明该阶段主要是内部扩散反应, Cs+在孔道内扩散, 占据吸附位点, 进行化学反应(Ding et al., 2013);第3阶段开始吸附速度变慢, 可能是吸附位点逐渐被占据, 与Cs+结合几率逐渐变小导致;到第4阶段, 反应逐渐达到平衡.由于吸附剂的载体成分PVA中含有大量的羟基官能团, 与H2O分子形成氢键相结合, 致使吸附剂表面形成了厚度较高且较为牢固的液膜(何维, 2015), 这使得达到反应平衡的时间较长.综上所述, AMP-PVA吸附Cs+为复杂的物理化学共同吸附过程, 主要包括表面吸附络合作用和层间离子交换作用, 但以后者占主导地位(孙胜龙等, 1999).
 |
| 图 6 AMP-PVA颗粒Cs+吸附动力学模型分析 (a.准一级动力学模型、准二级动力学模型, b.颗粒内扩散模型.c. Boyd准一级模型)(实验条件:C0=100 mg·L-1, 反应温度25 ℃, 反应时间0~48 h) Fig. 6 Kinetics model analysis of Cs+ adsorption by AMP-PVA (a.Pseudo-first-order, Pseudo-second-order, b. Intra-particle Diffusion Model, c. Boyd-pseudo-first Model) |
| 表 1 AMP-PVA的Cs+吸附动力学常数和可决系数 Table 1 Adsorption kinetic constants and their correlation coefficients of Cs+ adsorption on AMP-PVA |
等温吸附模型的参数可以说明吸附剂的表面特性, 阐释材料的吸附行为和性能.本研究采用经典的Langmuir模型(式(7))、Freundlich模型(式(8))和Dubinin-Radushkevich模型(式(9))拟合曲线.

|
(7) |

|
(8) |

|
(9) |
式中, qmax为固体材料对水中Cs+的理论最大吸附容量(mg·g-1);Ce为反应达到平衡状态时水中Cs+的浓度(mg·L-1);KL、KF分别为模型吸附平衡常数, 受固体吸附剂的吸附性能等影响;1/n与吸附能力成反比, 当0.1 < 1/n < 0.5时表明吸附行为容易发生, 当1/n>2时表示吸附难度较大;Qs为该吸附方程计算获得的吸附容量(mg·g-1);KDR参数主要受反应过程的平均自由能影响(mol2·kJ-2).
图 7为Langmuir、Freundlich和Dubinin-Radushkevich模型拟合的不同温度下AMP-PVA对Cs+的吸附平衡浓度变化情况, 相关参数列于表 3.总体而言, 在3种不同的温度下, 随着平衡浓度的增加, 吸附量有着相同的增加趋势.但由表 3可知, 不同温度下材料拟合的等温吸附模型不同.在15 ℃时拟合效果更接近Freundlich模型(R2=0.97), 说明该温度下吸附以多层吸附为主, 可能是由于低温条件下分子热运动相对较差, 吸附位点的占据不均匀所导致.Freundlich模型拟合结果表明, 在不同温度下, 1/n在0.1~1之间, 表明吸附过程可能受化学吸附控制且吸附过程较易进行(王君等, 2019).随着温度的升高, 吸附强度1/n值越大, 表明吸附过程吸附剂与吸附剂形成了较强的键(Ali et al., 2016).材料在25 ℃时应用Langmuir、Freundlich、Dubinin-Radushkevich模型拟合效果均较好(R2分别为0.9802、0.9793、0.9808).Langmuir吸附等温模型的良好拟合效果表明Cs+在AMP-PVA上的吸附为单层吸附, 说明Cs+的吸附是均匀地分布在AMP-PVA整个外部和内部表面上, 并且计算的RL在0~1之间表示这是一个有利的吸附过程(邓浩, 2017).Freundlich模型拟合效果较好表明该吸附过程为多层吸附, 这是因为该材料为颗粒状多层次的核壳结构, Cs+在经过物理扩散到PVA/TEOS交联的网状结构中之后, 又与AMP结合进行离子交换形成化学吸附, 从而导致热量的吸收与释放不一, 进而形成多层吸附.Dubinin-Radushkevich模型中E值大于8 kJ·mol-1, 说明该吸附过程受到物理吸附和离子交换的双重作用, 符合动力学拟合结果(Kilincarslan Kaygun et al., 2017).在35 ℃条件下Langmuir模型的拟合结果更好(R2=0.9520), 说明在较高温度条件下, 由于Cs+吸收更多热量, 导致热运动变得剧烈, 能够更加均匀的分布在AMP-PVA颗粒的内外表面.根据Langmuir模型拟合出的最大吸附量分别为93.63 mg·g-1(25 ℃)、109.56 mg·g-1(35 ℃), 随着温度的提高, 材料的吸附量有所提升, 进一步说明AMP-PVA对Cs+的吸附行为是自发、吸热、可持续的(胡冬雪等, 2019).
 |
| 图 7 AMP-PVA吸附Cs+的等温吸附模型分析 (a.Langmuir模型, b.Freundlich模型, c.Dubinin-Radushkevich模型)(实验条件:C0=0~220 mg·L-1, 反应温度25 ℃, 反应时间15 h) Fig. 7 Isotherms model analysis of Cs+ adsorption by AMP-PVA (a.Langmuir model, b.Freundlich model, c.Dubinin-Radushkevich model) |
| 表 2 不同温度下AMP-PVA的吸附等温线参数及其可决系数 Table 2 Adsorption isotherm parameters and their correlation coefficients of AMP-PVA at different temperatures |
| 表 3 AMP- PVA吸附Cs+前后的元素分析 Table 3 Changes of elements on the surface of AMP-PVA before and after adsorption |
制备所得复合材料AMP-PVA为不规则的浅绿色颗粒, 其扫描电镜分析结果如图 8所示.由图 8b、8c可知, AMP-PVA颗粒表面呈不规则形状的褶皱, 同时也存在一定量的孔洞形态;而制备的纯AMP为形状规则均匀的细颗粒态(图 8a), 是多面体形状的典型状态(Alcaniz-Monge et al., 2011).特征现象说明复合材料结构稳定性有所加强并具有多孔特性.将AMP负载到PVA-TEOS基质上后, 有一些不规则的块状颗粒, 这表明聚合物的网络约束效应对聚乙烯醇和二氧化硅基体的尺寸和形态产生了有效的影响, AMP颗粒有效地分散或沉积在多孔网状基质的外表面和内部孔道内.从图 8c和8d可清晰地看出材料吸附前后表面形貌变化, 但仍能观察到其表面有均匀分散的AMP小颗粒, 且吸附前后网状结构并无改变, 说明AMP-PVA在吸附Cs+过程中是相对稳定的.
 |
| 图 8 吸附材料的扫描电镜图像 (a.AMP, b~c.AMP-PVA, d.AMP-PVA-Cs) Fig. 8 SEM images of AMP(a), AMP-PVA(b, c) and AMP-PVA-Cs(d) |
AMP-PVA吸附前后的X射线能谱分析见图 9, 表面原子个数百分比见表 3.从表 3可以计算出, AMP-PVA中AMP的元素组成比例为P: Mo: O≈1:12:40, 符合[PMo12O40]3-, 从而可以得出在复合过程中并不会影响AMP的晶体结构.观察能谱图可发现在3.80、4.25、4.60、5.25 keV处出现了Cs的特征峰(张思月, 2018), 并由吸附前后元素变化情况可知, 吸附后N原子的个数百分比由6.44%减少至2.36%, 这表明Cs+被成功吸附在复合材料AMP-PVA表面, 推测其吸附机理可能是NH4+与Cs+发生离子交换反应, Cs+将NH4+从AMP的Keggin结构中置换出来.吸附前后材料的mapping图 10可证实了这一机理, 吸附前后N元素减少而新增了Cs元素(张晓霞, 2017).
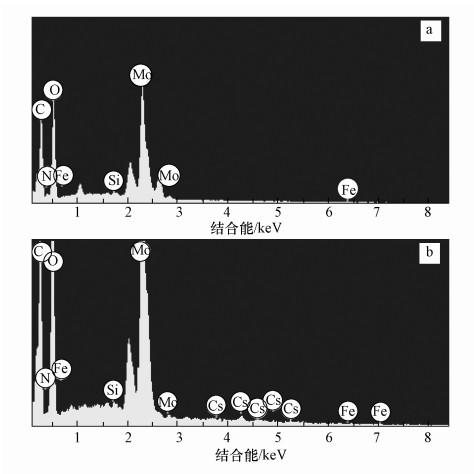 |
| 图 9 AMP- PVA吸附Cs+前(a)、后(b)的EDS谱 Fig. 9 EDS spectra of AMP、AMP-PVA before (a) and after (b) adsorption |
 |
| 图 10 AMP- PVA吸附Cs+前、后的元素分布 Fig. 10 EDS mapping of AMP、AMP-PVA before and after adsorption |
此外, 金属水合离子半径对吸附亲和力起到至关重要的决定性作用, 由于水合离子半径NH4+(3.31)与Cs+(3.29)相似, 使得二者可以顺利地进行离子交换(图 11);其次更为重要的是NH4+对于碱金属离子的吸附选择性顺序为Cs+>Rb+>K+>Na+>Li+, 因此, Cs+与NH4+的离子交换是具有最优先级的(Tan et al., 2016).从这两点可以看出AMP被公认为是具有高吸附量和选择性的吸附剂之一, 吸附过程可能是NH4+与Cs+之间的离子交换, 具体如图 11、式(10)所示.

|
(10) |
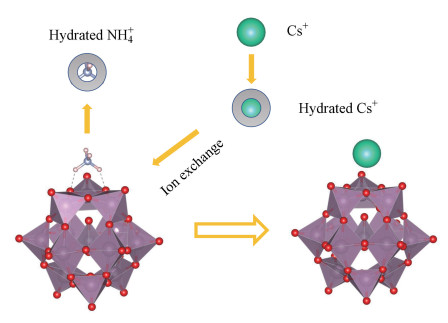 |
| 图 11 AMP-PVA用于去除水中Cs+的离子交换原理 Fig. 11 Ion exchange principle of removing Cs+ from aqueous solution by AMP- PVA |
AMP、AMP-PVA吸附前后的红外光谱如图 12所示.从图 12可以明显观察到AMP与AMP-PVA的光谱基本一致, 且大多数光谱的特征带都在低频光谱区(500~1600 cm-1), 这符合磷钼酸铵的Keggin结构(Ansari et al., 2020).在这一光谱区发现了各种类型的Mo—O键:964 cm-1(Mo—O)、862 cm-1(Mo—O—Mo, 共角八面体)、789 cm-1(Mo—O—Mo, 共边八面体)的吸收峰, 同时还存在P—O的振动带(1064 cm-1)和变形振动带(506 cm-1), 均为[PMo12O40]3-结构的特征峰(Katsoulis, 1998), 说明AMP中完整的[PMo12O40]3-Keggin结构已经负载在PVA-TEOS基质上, 形成了复合材料AMP-PVA.另外, 3443、1619 cm-1处出现的强峰对应AMP中—OH键的拉伸振动, 2925cm-1处为—CH2基团的伸缩振动(胡佩卓等, 2019).1064 cm-1为PVA中羟基与TEOS上硅氧基水解生成的Si—O—C键, 表明二者成功交联.在1407 cm-1区域发现的强峰是N—H的弯曲振动吸收峰, 表明NH4+的存在.对比AMP和AMP-PVA曲线再次说明AMP被完整地保留在复合材料中, 对比AMP-PVA、AMP-PVA-Cs曲线表明N—H的弯曲振动吸收峰较吸附前强度减小, 这进一步说明AMP-PVA对Cs+的特异性选择, 将结构中的NH4+置换出来, 实现了对Cs+的离子交换作用, 这进一步证实了EDS的分析结果(Tan et al., 2014).
 |
| 图 12 AMP、AMP-PVA吸附Cs+前后的红外光谱 Fig. 12 FT-IR of AMP, AMP-PVA before and after adsorption |
图 13为吸附Cs+前后AMP-PVA颗粒的XRD衍射分析图.由图 13可知, AMP-PVA颗粒的衍射峰线图中出现了一系列AMP的特征峰(2θ=10.8°、15.2°、21.6°、26.5°、30.7°、36.1°、55.7°), 为其八面立方体晶胞(晶胞参数a=1.1675 nm和α=90°)的(110)、(200)、(220)、(222)、(400)、(332)、(550)晶面(陈荧荧, 2017), 同时也出现了2θ=18.8°的PVA的特征峰, 说明合成的吸附材料同时含有AMP和PVA成分, 且AMP保持良好的晶型, 并在PVA-TEOS基质中稳定存在.进一步观察分析, 在2θ=20°~30°之间衍射峰形状平缓出现驼峰, 这是因为TEOS是硅胶基质的非晶体物质, 与此同时在2θ=43.9°(400)、57.8°(551)和62.7°(440)处得到了Fe3O4的特征峰(JCPDS 19-0629)(Thomas et al., 2006), 二者充分说明PVA、TEOS与Fe3O4良好地交联在一起并成功包埋AMP, 这与SEM的表征结果相同.比较分析吸附前后颗粒的特征峰分布及峰强变化, 发现吸附Cs+后的AMP-PVA-Cs特征曲线中, 特征峰分布并没有改变, 只是相应AMP特征峰有所减弱, 说明可能是AMP与Cs+发生离子交换反应的同时材料保持了良好的结构稳定性.
 |
| 图 13 吸附Cs+前后AMP-PVA磁性颗粒的X射线衍射图谱 Fig. 13 XRD pattern of AMP-PVA before and after adsorption |
为了探究AMP-PVA颗粒对Cs的吸附机理, 对吸附前后材料的XPS谱图进行分析, 结果如图 14所示.根据图 14a中吸附前后峰位对比发现, 吸附后AMP-PVA颗粒出现了明显的Cs 3d特征峰, 这表明Cs被成功吸附;放大观察发现其Cs 3d5和Cs 3d3的特征峰, 其中, Cs 3d5的结合能为723.25 eV(图 14b).Morgan等(1973)研究表明, 当3d5结合能在723.8 eV附近时有Cs的磷酸结合态物质生成, 这说明Cs+进入吸附材料后成功与AMP中的[PMo12O40]3-结合.为了进一步证明Cs+是与[PMo12O40]3-发生反应, 研究了吸附前后Mo 3p轨道与N1s轨道分峰图.由图 14c、14d可知, 吸附前Mo 3p3轨道结合能为398.78 eV, Mo 3p1结合能为416.25 eV, 吸附后分别为398.86 eV和416.71 eV, 同时还发现O的1s轨道结合能从532.31 eV变为532.50 eV, Mo与O的结合能均增大, 这表明发生吸附反应对Mo—O键有一定的影响(Benoist et al., 1995).除此之外, 对比吸附前后发现N 1s轨道的峰强明显减弱, 进一步证明被AMP-PVA颗粒吸附的Cs+与NH4+发生了离子交换反应, 使得材料中的NH4+浓度减弱.
 |
| 图 14 X射线光电子能谱 (a.扫描全谱图, b.AMP-PVA吸附Cs的3d3和3d5分峰谱, c.吸附前AMP-PVA中Mo 3p谱、N 1s谱, d.吸附后AMP-PVA中Mo 3p谱、N1s谱) Fig. 14 XPS wide scan patterns (a), Cs 3d3 and 3d5 spectra of AMP-PVA (b), Mo 3p and N1s spectra of AMP-PVA before adsorption (c) and Mo 3p and N1s spectra of AMP-PVA after adsorption (d) |
AMP-PVA复合材料的TGA-DSC分析表明了材料的分解步骤, 结果如图 15所示.TG曲线显示随着温度的上升, 材料的质量逐渐发生变化, 主要表现为3个失重步骤/过程.第1阶段在100 ℃之前, 质量损失(3.02%)归因于材料失去了自由水和吸附水的解吸(王启龙, 2014);在100~450 ℃之间质量损失(21.94%)分两步进行, 一部分是由于失去结晶水, 另一部分主要由于聚合物的交换结构中失去了铵根离子并分解产生氨气, 并伴随热量的释放;第3阶段发生在450 ℃以后, 失重11.45%, 原因主要是稳定的Keggin结构被破坏, 生成磷化合物和钼化合物(刘珊, 2012).对比纯AMP和AMP-PVA的TG曲线可知, AMP负载基质后在450 ℃之前损失增多(从约损失12%下降到损失约30%), 可能是由于AMP复合到PVA-TEOS基质后, 去除了吸附在网状基质中的水, 因为与无孔的本体AMP相比, 基质具有保留更多水的趋势和可能.除此以外, 对比AMP与AMP-PVA在400~500 ℃以后的质量损失发现, AMP在该温度段内的质量几乎没有损失, 而AMP-PVA却损失了约8%的质量, 可能是由于PVA-TEOS基质中碳元素的损失(Ingale et al., 2014).然而, 由于放射性废水的去除一般在常温下进行, AMP-PVA在100 ℃之前仍保持良好的结构和稳定性, 所以此复合材料可以以稳定结构应用于水中Cs+的去除.
 |
| 图 15 AMP(a)和AMP-PVA(b)的热重-差热分析图 Fig. 15 TG-DSC of AMP(a) and AMP-PVA(b) |
图 16为AMP-PVA的磁滞回线图, 测得其饱和磁化强度(Ms)为4.16 emu·g-1, 剩余强化强度(Mr)为2.69 emu·g-1, 由此可知这两种材料均能进行良好的磁分离.AMP-PVA中的Fe3O4通过TEOS与PVA连接, 在反应中SiO2对纳米Fe3O4颗粒产生包裹, 较厚的SiO2壳会减弱颗粒之间的偶极-偶极相互作用, 并减少颗粒聚集, 致使Fe3O4的磁性减弱(杨姗也等, 2018).
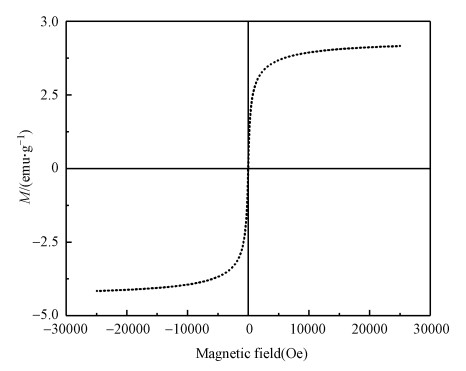 |
| 图 16 AMP-PVA磁滞回线谱图 Fig. 16 Hystersis loops for AMP-PVA composite |
利用不同浓度的NH4NO3溶液探究材料解析的最佳条件, 同时增加了不同循环次数下材料对Cs去除性能的影响评价, 实验结果如图 17所示.图 17a为不同浓度下NH4+解吸液对AMP-PVA的解吸效果图.由图可知, 随着NH4+浓度的增加, 解吸率逐渐增加, 当NH4+浓度由0.1 mol·L-1上升到1 mol·L-1时, 解吸率由不足10%上升到65%.这是因为NH4+与吸附在材料中的Cs+有离子交换作用.图 17b为不同循环次数下AMP-PVA对Cs+的去除效果.由于解析实验中材料的浸出和活化位点的损失(Yang et al., 2017), 随着循环次数的增加, 吸附能力有所下降, 循环4次后去除率由60%下降到近50%.但总的来说, AMP-PVA可用于放射性废水除Cs的循环使用.
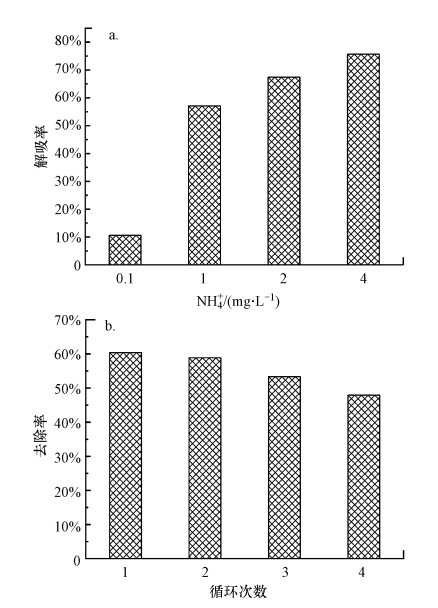 |
| 图 17 AMP-PVA在不同NH4+浓度下解吸率(a)及AMP-PVA的循环再生效果(b) (实验条件:c(Cs+)=200 mg·L-1, 反应温度25 ℃, 反应时间15 h, 固液比1 g·L-1) Fig. 17 Desorption of AMP-PVA under different concentrations of ammonium ions (a) and reusing of AMP-PVA composite(b) |
通过文献调研的研究现状来看, 用于水中Cs去除的吸附材料主要包括普鲁士蓝类似物、杂多酸盐、粘土矿物、金属硫化物.由于理化性质的差异, 导致其去除效果和性能不具有可比性.但与本研究中相同主体材料的AMP类复合材料比较, 进而评价其在实际场地的应用性能是具有科学意义的.为了防止细粉状AMP的流失, 许多研究均致力于利用有机和无机材料作为基底制备复合材料.如Banerjee等(2008)将AMP固定在聚甲基丙烯酸甲酯中合成AMP-PMMA用于从酸性溶液中去除Cs+, 颗粒尺寸相比于AMP显著增大, 但对Cs的吸附量从125.0 mg·g-1下降到33.2 mg·g-1;Ye等(2009)将海藻酸钠与AMP包裹, 制备了AMP-ALG小球, 具有良好的亲水性, 最大吸附量可达到91.7 mg·g-1, 但ALG的水力学性能较差, 可能会发生破裂;张思月等(2018)以Zn2+为交联剂, 将AMP包埋于果胶中, 制备了果胶/AMP-Zn微球吸附剂, 最大吸附量为41.837 mg·g-1.经过对比可知, 本研究制备的AMP-PVA复合材料的最大吸附量为109.56 mg·g-1, 吸附平衡时间约为30 h, 受温度影响并不明显, 在强酸性条件下仍有良好的吸附效果和选择性, 同时材料稳定的结构可用于柱操作, 但仍可以提升其磁分离性能和吸附容量, 降低制备成本并简化合成步骤, 使其具备更大的高效吸附潜力和实际应用能力.这对探索其在环境修复中的广泛应用具有重要意义.
4 结论(Conclusions)1) 采用溶胶-凝胶沉淀法成功制备了AMP-PVA复合离子交换吸附剂.静态实验表明, 在308 K、pH=7.7时, AMP-PVA对Cs+的吸附量最大为109.56 mg·g-1.特别的是, AMP-PVA在强酸条件下仍保持对Cs+良好的选择性去除效果.
2) AMP-PVA对Cs+的吸附过程符合准二级动力学模型, 属于化学吸附控制过程, 同时内扩散和Boyd模型表明该吸附过程受液膜扩散、表面吸附、颗粒内扩散等因素共同影响.Freundlich方程能更好地模拟吸附等温线, 表明该吸附过程是以多分子层吸附为主, 且自发、吸热、可持续.
3) 碳酸钠的添加量会影响AMP-PVA的多孔结构, 其主要体现在孔径分布上, 并且在一定范围内介孔数量占比越大, 材料的吸附效果越好.
4) SEM-EDS、XRD、BET综合表征结果表明, PVA-TEOS多孔基质有效地负载了AMP颗粒, AMP-PVA复合材料为颗粒态网片状夹缝孔结构, 与纯AMP相比具有更紧密的交联网络, 且吸附前后材料结构未发生明显改变;对比吸附前后FTIR光谱发现N—H振动峰减弱, 说明NH4+参与了Cs+的吸附过程;XPS表征吸附过程与Mo—O键有一定的影响, N 1s轨道峰强减弱也有效地说明了AMP-PVA的主要作用机制可能是AMP中的NH4+与Cs+发生了离子交换反应.
Alcañiz-Monge J, Trautwein G, Román-Martínez M C. 2011. Effect of counteranion of ammonium salts on the synthesis of porous nanoparticles (NH4)3[PMo12O40][J]. Solid State Sciences, 13(1): 30-37. DOI:10.1016/j.solidstatesciences.2010.10.002 |
Ali R M, Hamad H A, Hussein M M, et al. 2016. Potential of using green adsorbent of heavy metal removal from aqueous solutions: Adsorption kinetics, isotherm, thermodynamic, mechanism and economic analysis[J]. Ecological Engineering, 91: 317-332. DOI:10.1016/j.ecoleng.2016.03.015 |
Ansari S A, Sahoo G C, Dey S, et al. 2020. Radiation stability of ceramic tubular membranes containing ammonium molybdophosphate (AMP) for the application of radio-cesium recovery from radioactive wastes[J]. Journal of Radioanalytical and Nuclear Chemistry, 326(3): 1631-1638. DOI:10.1007/s10967-020-07449-2 |
Aoyama M. 1988. Evidence of stratospheric fallout of caesium isotopes from the Chernobyl accident[J]. Geophysical Research Letters, 15(4): 327-330. DOI:10.1029/GL015i004p00327 |
Banerjee D, Rao M A, Gabriel J, et al. 2008a. Recovery of purified radiocesium from acidic solution using ammonium molybdophosphate and resorcinol formaldehyde polycondensate resin[J]. Desalination, 232(1/3): 172-180. |
Banerjee D, Rao M A, Gabriel J, et al. 2008b. Recovery of purified radiocesium from acidic solution using ammonium molybdophosphate and resorcinol formaldehyde polycondensate resin[J]. Desalination, 232(1): 172-180. |
Benoist L, Gonbeau D, Pfister-Guillouzo G, et al. 1995. XPS analysis of oxido-reduction mechanisms during lithium intercalation in amorphous molybdenum oxysulfide thin films[J]. Solid State Ionics, 76(1): 81-89. |
Buchwald H, Thistlethwaite W P. 1958. Some cation exchange properties of ammonium 12-molybdophosphate[J]. Journal of Inorganic and Nuclear Chemistry, 5(4): 341-343. DOI:10.1016/0022-1902(58)80013-5 |
蔡璇, 刘燕, 张云, 等. 2012. 核事故产生的放射性废水处理方法研究进展[J]. 化学通报, 75(6): 483-488. |
Chakravarty R, Ram R, Pillai K T, et al. 2012. Ammonium molybdophosphate impregnated alumina microspheres as a new generation sorbent for chromatographic 137Cs/(137m)Ba generator[J]. J Chromatogr A, 1220: 82-91. DOI:10.1016/j.chroma.2011.11.059 |
陈荧荧. 2017. 磷钼酸铵复合材料的制备及其性能研究[D]. 长春: 长春理工大学. 54
|
Chen S, Hu J, Han S, et al. 2020. A review on emerging composite materials for cesium adsorption and environmental remediation on the latest decade[J]. Separation and Purification Technology, 251: 117340. DOI:10.1016/j.seppur.2020.117340 |
Clarke T D, Wai C M. 1998. Selective removal of cesium from Acid solutions with immobilized copper ferrocyanide[J]. Anal Chem, 70(17): 3708-3711. DOI:10.1021/ac971138b |
Dan H, Xian Q, Chen L, et al. 2019. One-step direct synthesis of mesoporous AMP/SBA-15 using PMA as acid media and its use in cesium ion removal[J]. Journal of Nuclear Materials, 527: 151809. DOI:10.1016/j.jnucmat.2019.151809 |
邓浩. 2017. 磷钼酸铵/硅胶基质复合无机离子交换剂的制备与性能研究[D]. 绵阳: 西南科技大学. 87
|
Deng H, Li Y, Huang Y, et al. 2016. An efficient composite ion exchanger of silica matrix impregnated with ammonium molybdophosphate for cesium uptake from aqueous solution[J]. Chemical Engineering Journal, 286: 25-35. DOI:10.1016/j.cej.2015.10.040 |
Deng H, Li Y, Wu L, et al. 2017. The novel composite mechanism of ammonium molybdophosphate loaded on silica matrix and its ion exchange breakthrough curves for cesium[J]. Journal of Hazardous Materials, 324: 348-356. DOI:10.1016/j.jhazmat.2016.10.068 |
Ding D, Zhao Y, Yang S, et al. 2013. Adsorption of cesium from aqueous solution using agricultural residue - Walnut shell: Equilibrium, kinetic and thermodynamic modeling studies[J]. Water Research, 47(7): 2563-2571. DOI:10.1016/j.watres.2013.02.014 |
Flory P J, Krigbaum W R. 1950. Statistical mechanics of dilute polymer solutions II[J]. The Journal of Chemical Physics, 18(8): 1086-1094. DOI:10.1063/1.1747866 |
耿旭, 杨明. 2017. 新型Ag(I)选择性吸附材料的制备及吸附性能研究[J]. 环境科学学报, 37(9): 3381-3389. |
Hassan C M, Peppas N A. 2000. Structure and morphology of freeze/thawed PVA hydrogels[J]. Macromolecules, 33(7): 2472-2479. DOI:10.1021/ma9907587 |
何维. 2015. 完全醇解型PVA包装薄膜的耐水性研究[D]. 株洲: 湖南工业大学
|
Holdsworth, Eccles, Rowbotham, et al. 2019. The effect of gamma irradiation on the ion exchange properties of caesium-selective ammonium Phosphomolybdate-Polyacrylonitrile (AMP-PAN) composites under spent fuel recycling conditions[J]. Separations, 6(2): 23. DOI:10.3390/separations6020023 |
胡冬雪, 张飞杰, 周燕, 等. 2019. 腐殖酸负载羟基磷灰石对废水中Cd2+吸附性能的影响[J]. 环境科学学报, 39(12): 4022-4030. |
胡佩卓, 刘莲, 王海静, 等. 2019. 磷钼酸铵/聚丙烯酸复合凝胶吸附剂的合成及对铯的分离[J]. 核化学与放射化学, 41(4): 361-369. |
黄园英, 王倩, 汤奇峰, 等. 2019. 纳米铁去除水体中镉的反应动力学、吸附平衡和影响因素[J]. 生态环境学报, 28(10): 2053-2061. |
黄召亚, 张东, 谭昭怡. 2013. 沉淀法制备磷钼酸铵及其对Cs+的吸附特性研究[J]. 核技术, 36(2): 44-47. |
Ingale S V, Ram R, Sastry P U, et al. 2014. Synthesis and characterization of ammonium molybdophosphate-silica nano-composite (AMP-SiO2) as a prospective sorbent for the separation of 137Cs from nuclear waste[J]. Journal of Radioanalytical and Nuclear Chemistry, 301(2): 409-415. DOI:10.1007/s10967-014-3143-9 |
Katsoulis D E. 1998. A survey of applications of polyoxometalates[J]. Chemical Reviews, 98(1): 359-388. |
Kilincarslan Kaygun A, Eral M, Akyil Erenturk S. 2017. Removal of cesium and strontium using natural attapulgite: evaluation of adsorption isotherm and thermodynamic data[J]. Journal of Radioanalytical and Nuclear Chemistry, 311(2): 1459-1464. DOI:10.1007/s10967-016-4989-9 |
Klaysom C, Moon S H, Ladewig B P, et al. 2011. The effects of aspect ratio of inorganic fillers on the structure and property of composite ion-exchange membranes[J]. Journal Colloid Interface Science, 363(2): 431-439. DOI:10.1016/j.jcis.2011.07.071 |
梁成强, 贾铭椿, 王晓伟, 等. 2019. 层状金属硫化物硫化锡钾的制备及其对Sr2+的吸附性能研究[J]. 原子能科学技术, 53(11): 2141-2147. DOI:10.7538/yzk.2018.youxian.0907 |
刘珊. 2012. 粗粒磷钼酸铵及其复合物对铷/铯离子的选择性吸附研究[D]. 长沙: 湖南大学. 78
|
Morgan W E, Stec W J, Van Wazer J R. 1973. Inner-orbital binding-energy shifts of antimony and bismuth compounds[J]. Inorganic Chemistry, 12(4): 953-955. DOI:10.1021/ic50122a054 |
Park Y, Shin W S, Choi S. 2013. Ammonium salt of heteropoly acid immobilized on mesoporous silica (SBA-15): An efficient ion exchanger for cesium ion[J]. Chemical Engineering Journal, 220: 204-213. DOI:10.1016/j.cej.2013.01.027 |
Querfeld R, Pasi A, Shozugawa K, et al. 2019. Radionuclides in surface waters around the damaged Fukushima Daiichi NPP one month after the accident: Evidence of significant tritium release into the environment[J]. Science of the Total Environment, 689: 451-456. DOI:10.1016/j.scitotenv.2019.06.362 |
饶本强, 张少丽, 李勇, 等. 2020. PVA-膨润土包埋固定化荒漠丝状蓝藻复合体的制备及其对Cu(Ⅱ)的吸附特性[J]. 环境科学学报, 40(11): 3939-3949. |
Rojas F, Kornhauser I, Felipe C, et al. 2002. Capillary condensation in heterogeneous mesoporous networks consisting of variable connectivity and pore-size correlation[J]. Physical Chemistry Chemical Physics, 4(11): 2346-2355. DOI:10.1039/b108785a |
Smit J V R. 1958. Ammonium Salts of the Heteropolyacids as cation exchangers[J]. Nature, 181(4622): 1530-1531. DOI:10.1038/1811530a0 |
孙胜龙, 赵晓明. 1999. 钠、铝改造型膨润土对溶液中Cr(Ⅵ)吸附及其机理研究[J]. 水处理技术, (6): 344-349. DOI:10.3969/j.issn.1000-3770.1999.06.007 |
Tan Z, Dong L, Huang Z, et al. 2016. A theoretical study on the selective adsorption of NH4+ and Cs+ on the phosphomolybdate ion[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 502: 74-80. |
Thomas S, Sakthikumar D, Joy P A, et al. 2006. Optically transparent magnetic nanocomposites based on encapsulated Fe3O4 nanoparticles in a sol-gel silica network[J]. Nanotechnology, 17(22): 5565-5572. DOI:10.1088/0957-4484/17/22/007 |
Tranter T J, Herbst R S, Todd T A, et al. 2002. Evaluation of ammonium molybdophosphate-polyacrylonitrile (AMP-PAN) as a cesium selective sorbent for the removal of 137Cs from acidic nuclear waste solutions[J]. Advances in Environmental Research, 6(2): 107-121. DOI:10.1016/S1093-0191(00)00073-3 |
van der Merwe A. 2019. Nuclear energy saves lives[J]. Nature, 570(7759): 36. |
王君, 周怡伶, 陈勇, 等. 2019. Fe3O4@SiO2-Chitosan的制备及其对水中Cu2+的吸附效能研究[J]. 环境科学学报, 39(8): 2567-2574. |
王启龙. 2014. 多孔性硅基磷钼酸铵吸附剂的合成及其对铯的吸附研究[D]. 上海: 上海交通大学. 89
|
徐世平, 张继荣, 宋崇立. 2000. 用无机离子交换法从酸性高放废液中去除铯研究进展[J]. 辐射防护通讯, (6): 8-12. |
Yang D, Sarina S, Zhu H, et al. 2011. Capture of radioactive Cesium and iodide ions from water by using titanate nanofibers and nanotubes[J]. Angewandte Chemie International Edition, 50(45): 10594-10598. DOI:10.1002/anie.201103286 |
Yang H, Yu H, Sun J, et al. 2017. Facile synthesis of mesoporous magnetic AMP polyhedric composites for rapid and highly efficient separation of Cs + from water[J]. Chemical Engineering Journal, 317: 533-543. DOI:10.1016/j.cej.2017.02.088 |
杨姗也, 王祥学, 陈中山, 等. 2018. 四氧化三铁基纳米材料制备及对放射性元素和重金属离子的去除[J]. 化学进展, 30(Z1): 225-242. |
Ye X, Wu Z, Li W, et al. 2009. Rubidium and cesium ion adsorption by an ammonium molybdophosphate-calcium alginate composite adsorbent[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 342(1/3): 76-83. |
Zhang N, Chen S, Hu J, et al. 2020. Robust and recyclable sodium carboxymethyl cellulose-ammonium phosphomolybdate composites for cesium removal from wastewater[J]. RSC Advances, 10(11): 6139-6145. DOI:10.1039/C9RA09803H |
张思月. 2018. 果胶基微球的制备及对钍和铯吸附性能研究[D]. 绵阳: 西南科技大学. 82
|
张晓霞. 2017. 多孔性硅基磷钼酸铵吸附剂对裂变产物铯的吸附及固化性能研究[D]. 上海: 上海交通大学. 144
|
Tan Z, Huang Z, Zhang D, et al. 2014. Structural characterization of ammonium molybdophosphate with different amount of cesium adsorption[J]. Journal of Radioanalytical and Nuclear Chemistry, 299(3): 1165-1169. DOI:10.1007/s10967-013-2843-x |
Zhou Q, Lin X, Li B, et al. 2014. Fluoride adsorption from aqueous solution by aluminum alginate particles prepared via electrostatic spinning device[J]. Chemical Engineering Journal, 256: 306-315. DOI:10.1016/j.cej.2014.06.101 |
Zong Y, Zhang Y, Lin X, et al. 2017. Preparation of a novel microsphere adsorbent of prussian blue capsulated in carboxymethyl cellulose sodium for Cs(I) removal from contaminated water[J]. Journal of Radioanalytical and Nuclear Chemistry, 311(3): 1577-1591. DOI:10.1007/s10967-016-5111-z |
 2021, Vol. 41
2021, Vol. 41


